题目内容
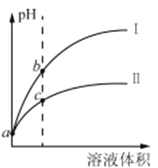
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4–)+ c(C2O42–)=0.100 mol·L–1的H2C2O4和NaOH混合的溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A. pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)>c(HC2O4–)
B. pH=7的溶液中:c(Na+)= 2c(C2O42–)
C. c(HC2O4–)= c(C2O42–)的溶液中:c(Na+)>0.100 mol·L–1+ c(HC2O4–)
D. c(Na+)=0.100 mol·L–1的溶液中:c(H+)+c(H2C2O4)=c(OH–)+c(C2O42–)
【答案】D
【解析】A、由图可以看出,pH=2.5时,c(H2C2O4)<0.02mol/L,c(C2O42-)<0.02mol/L,c(HC2O4-)>0.08mol/L,则c(H2C2O4)+ c(C2O42-)< c(HC2O4-),A项错误;B、根据电荷守恒得c(Na+)+ c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),pH=7.0时,c(H+)= c(OH-),则c(Na+)= c(HC2O4-)+2c(C2O42-),即c(Na+)>2c(C2O42-),B项错误;C、根据c(Na+)+ c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-)且c(HC2O4-)+c(C2O42-)+ c(H2C2O4)=0.100mol/L,结合c(HC2O4-)= c(C2O42-)可得c(Na+)=0.100mol/L-c(HC2O4-)+c(H2C2O4)+c(OH-)-c(H+),由图可知c(HC2O4-)=c(C2O42-)时,溶液pH<7显酸性,则c(Na+)<0.100mol/L +c(HC2O4-), C项错误;D、c(Na+)=0.100mol/L时,则有c(Na+) =c(HC2O4-)+c(C2O42-)+ c(H2C2O4),溶液中根据电荷守恒可得c(Na+)+ c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),二式结合可得c(H+)+c(H2C2O4)= c(C2O42-)+c(OH-),D项正确;答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案