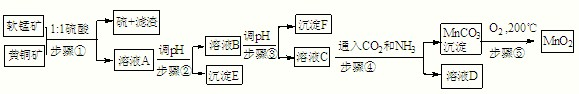
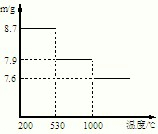
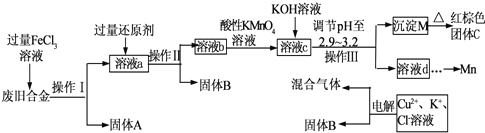
��Ŀ����
��10�֣���֪KMnO4��MnO2�����������¾��ܽ������ƣ�Na2C2O4��������
2MnO4����5C2O42����16H����2Mn2����10CO2����8H2O
MnO2��C2O42����4H����Mn2����2CO2����2H2O
ij�о�С��Ϊ�ⶨij���̿���MnO2������������ȷ��ȡ1.20g���̿���Ʒ������2.68g�����ƹ��壬�ټ���������ϡ���Ტ���ȣ����ʲ��μӷ�Ӧ������ַ�Ӧ֮����ȴ����ȥ���ʣ���������Һת�Ƶ�����ƿ�в����ݣ�����ȡ��25.00mL����Һ������ƿ�У�����0.0200mol��L��1KMnO4����Һ���еζ���������20.00mLKMnO4��Һʱǡ����ȫ��Ӧ���Իش��������⣺
��0.0200mol��L��1KMnO4����ҺӦ���� ��ѡ��ס����ҡ����ζ����У��ζ��յ�����ж� ��
�����ܷ�������о�С��������̿���MnO2���������� ��ѡ��ܡ��������ش��ܡ�������������� �����ش𡰷���˵��ԭ�� ��
������ʵ������д������в��������л�ʹ����MnO2����������ƫС���� ��
| A����Һת��������ƿ�У�δ���ձ�������ϴ�� |
| B���ζ�ǰ���첿����һ���ݣ��ζ��յ�ʱ��ʧ |
| C������ʱ�����ӿ̶��� |
| D���ζ�ǰ���Ӷ������ζ����Ӷ��� |
�ż� ����������1��KMnO4��Һ����ƿ����Һ��������Ϻ�ɫ���Ұ�����ڲ���ɫ�����ﵽ�ζ��յ� �Ʒ� ��Ϊ��֪������ƿ�Ĺ�� ��BC
����

| Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | Zn��OH��2 | Mn��OH��2 | |
| ��ʼ������pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| ������ȫ��pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
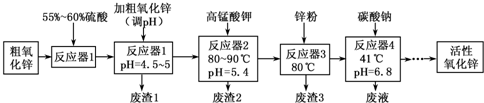
��1��������1������Ҫ�ɷ���
��2����ɡ���Ӧ��2���з�Ӧ֮һ�����ӷ���ʽ��
��3��պȡ����Ӧ��2���е���Һ����
��4��������2���������MnO2��������ȡMnO����֪��
2MnO2��s��+C��s��=2MnO��s��+CO2��g����H=-174.6kJ?mol-1
C��s��+CO2��g��=2CO��g����H=+283.0kJ?mol-1
��д��MnO2��s����CO��g����Ӧ��ȡMnO��s�����Ȼ�ѧ����ʽ��
��5������Ӧ��3���м���п�۵�������
��6������Ӧ��4���õ��ķ�Һ�У����е���Ҫ���ӳ���Na+�⣬����
��7���ӡ���Ӧ��4���о����˵Ȳ����õ���ʽ̼��п��ȡ��ʽ̼��п3.41g����400��450���¼��������أ��õ�ZnO 2.43g�ͱ�״����CO2 0.224L����ʽ̼��п�Ļ�ѧʽΪ