题目内容
将0.08 mol KMnO4固体(质量为12.64 g)加热一段时间后(已知KMnO4的分解率为x),收集到a mol O2;向反应后残留的固体中加入足量的浓盐酸,加热,又收集到b mol Cl2,此时Mn元素全部以Mn2+的形式存在于溶液中.
(1)请配平下列方程式:

(2)在上式反应中若收集到3.36 L Cl2(标准状况下)时,转移电子的物质的量为________.
(3)a+b=________(用含x的表达式表示).
(4)当a+b=0.18时,残留固体的质量为________
答案:
解析:
解析:
|
(1)1 8 2 1 2 4 (2)0.3 mol (3)0.2-0.04x (4)12 g(每空2分) |

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
| (2013?合肥一模)在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 5min末达到平衡,有关数据如表.
|
10mL含有0.020mol Na2CO3的溶液和20mL盐酸,不管是将前者加入后者中,还是将后者加入前者中,都有气体产生,但最终产生的气体体积不同,则盐酸的浓度合理的是( )
| A、0.05 mol?L-1 | B、0.08 mol?L-1 | C、1.60 mol?L-1 | D、2.00 mol?L-1 |
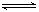 2NH3(g) ΔH<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) ΔH<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: