题目内容
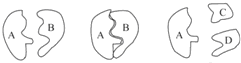
在一定条件下可实现如图所示物质之间的相互转化:

(1)根据你的推测,填写下列物质的化学式:
A. ;B. ;C. ;D. .
(2)简要说明A可转变为B和C的原因,写出有关的化学方程式: .
(3)写出E气体与A溶液反应的离子方程式: .

(1)根据你的推测,填写下列物质的化学式:
A.
(2)简要说明A可转变为B和C的原因,写出有关的化学方程式:
(3)写出E气体与A溶液反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:B加入硝酸银生成白色沉淀,说明B中含有Cl元素,则A中含有Cl元素,含A的水溶液加入苯酚变成紫色溶液,说明A为FeCl3,则FeCl3?6H2O在加热时水解可生成HCl和Fe(OH)3,可知B为HCl,C为Fe(OH)3,E为臭鸡蛋气味的气体,应为H2S,H2S与FeCl3发生氧化还原反应,方程式为2FeCl3+H2S=2HCl+S↓+2FeCl2,由此可知F为FeCl2,G为Fe,H为S,D为FeS,结合对应物质的性质以及题目要求解答该题.
解答:
解:B加入硝酸银生成白色沉淀,说明B中含有Cl元素,则A中含有Cl元素,含A的水溶液加入苯酚变成紫色溶液,说明A为FeCl3,则FeCl3?6H2O在加热时水解可生成HCl和Fe(OH)3,可知B为HCl,C为Fe(OH)3,E为臭鸡蛋气味的气体,应为H2S,H2S与FeCl3发生氧化还原反应,方程式为2FeCl3+H2S=2HCl+S↓+2FeCl2,由此可知F为FeCl2,G为Fe,H为S,D为FeS,
(1)由以上分析可知A为FeCl3,B为HCl,C为Fe(OH)3,D为FeS,故答案为:FeCl3;HCl;Fe(OH)3;FeS;
(2)A为FeCl3,FeCl3?6H2O在加热时水解可生成HCl和Fe(OH)3,反应的方程式为FeCl3?6H2O
Fe(OH)3+3HCl+3H2O,
故答案为:FeCl3?6H2O
Fe(OH)3+3HCl+3H2O;
(3)E气体与A溶液反应的离子方程式为2Fe3++H2S=2H++S↓+2Fe2+,故答案为:2Fe3++H2S=2H++S↓+2Fe2+.
(1)由以上分析可知A为FeCl3,B为HCl,C为Fe(OH)3,D为FeS,故答案为:FeCl3;HCl;Fe(OH)3;FeS;
(2)A为FeCl3,FeCl3?6H2O在加热时水解可生成HCl和Fe(OH)3,反应的方程式为FeCl3?6H2O
| ||
故答案为:FeCl3?6H2O
| ||
(3)E气体与A溶液反应的离子方程式为2Fe3++H2S=2H++S↓+2Fe2+,故答案为:2Fe3++H2S=2H++S↓+2Fe2+.
点评:本题是无机框图推断题,考查物质推断与性质,难度中等,掌握元素化合物的性质是解题的关键,注意特殊的颜色与特殊反应是推断的突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化合物中,含有共价键的是( )
| A、NaCl |
| B、He |
| C、NaOH |
| D、CaCl2 |
下列四个图示中,属于过滤操作的是( )
A、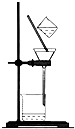 |
B、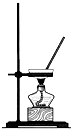 |
C、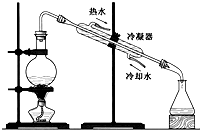 |
D、 |
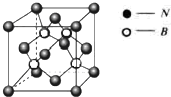 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.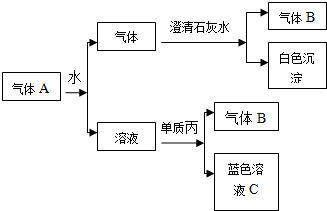 将红热固体单质甲放在显黄色的溶液乙中剧烈反应,产生混合气体A,A在常温下(不与空气接触)有如下变化:
将红热固体单质甲放在显黄色的溶液乙中剧烈反应,产生混合气体A,A在常温下(不与空气接触)有如下变化: