题目内容
下列四个图示中,属于过滤操作的是( )
A、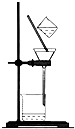 |
B、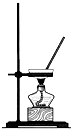 |
C、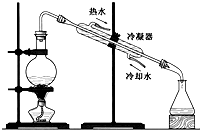 |
D、 |
考点:过滤
专题:化学实验基本操作
分析:A.该装置可分离难溶性固体和液体,是过滤装置;
B.该装置可分离可溶性固体和水,是蒸发装置;
C.该装置可分离相互溶解的液体,是蒸馏装置;
D.该装置可分离互不相溶的液体,是分液装置.
B.该装置可分离可溶性固体和水,是蒸发装置;
C.该装置可分离相互溶解的液体,是蒸馏装置;
D.该装置可分离互不相溶的液体,是分液装置.
解答:
解:A.该装置利用重力进行分离难溶于水的固体和液体,是过滤装置,故A正确;
B.该装置利用溶剂加热挥发,剩下的为固体,可分离可溶性固体和水,是蒸发装置,故B错误;
C.冷凝器是将通过的气体冷却变为液体,实现了互溶但沸点不同的液体的分离,是蒸馏装置,故C错误;
D.该装置中的分液漏斗为分离互不相溶的液体,是分液装置,故D错误;
故选A.
B.该装置利用溶剂加热挥发,剩下的为固体,可分离可溶性固体和水,是蒸发装置,故B错误;
C.冷凝器是将通过的气体冷却变为液体,实现了互溶但沸点不同的液体的分离,是蒸馏装置,故C错误;
D.该装置中的分液漏斗为分离互不相溶的液体,是分液装置,故D错误;
故选A.
点评:本题考查了化学实验的基本操作过滤,抓住过滤的原理进行解答是解题的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
二氧化硅的化学性质很不活泼,几乎所有的酸都不与其反应,但有一种酸能够和二氧化硅发生反应,这种酸是( )
| A、浓盐酸 | B、硫酸 |
| C、硝酸 | D、氢氟酸 |
下列各组物质的鉴别方法正确的是( )
①用新制的Cu(OH)2浊液鉴别甲酸、乙酸、乙醇;
②用溴水鉴别己烷、己烯、己炔;
③用FeCl3溶液鉴别苯、四氯化碳、苯酚;
④用硝酸银溶液鉴别氯苯、溴苯、碘甲烷.
①用新制的Cu(OH)2浊液鉴别甲酸、乙酸、乙醇;
②用溴水鉴别己烷、己烯、己炔;
③用FeCl3溶液鉴别苯、四氯化碳、苯酚;
④用硝酸银溶液鉴别氯苯、溴苯、碘甲烷.
| A、①②③④ | B、①③④ |
| C、①③ | D、②③④ |
下列事实能说明氯的非金属性比硫强的是( )
| A、铁与硫反应生成硫化亚铁,而铁与氯气反应时生成氯化铁 |
| B、与金属钠反应,氯原子得一个电子,而硫原子能得两个电子 |
| C、常温时氯气呈气态,而硫呈现固态 |
| D、氯的最高价为+7价,而硫的最高价为+6价 |
可逆反应2NO2(g)?N2O4(g)△H<0,试根据下列图象,判断t2,t3,t4时刻采取的措施是( )


| A、加入NO2、升高温度、增大压强 |
| B、加入N2O4、减小压强、加催化剂 |
| C、加入NO2、降低温度、减小压强 |
| D、加入N2O4、降低温度、加催化剂 |
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构.下列关于X、Y、Z、W四种元素的描述,正确的是( )
| A、原子半径:X>Y>Z>W |
| B、原子序数:Y>X>W>Z |
| C、原子最外层电子数:Y>X>Z>W |
| D、金属性:X>Y,还原性:W2->Z- |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol/L) | 0.05 | 0.15 | 0.1 |
| A、反应达到平衡时,X的转化率为50% | ||
B、反应可表示为X+Y?2Z,其平衡常数为
| ||
| C、若该反应为放热反应,升高温度,平衡常数减小 | ||
| D、增大压强使平衡向生成Z的方向移动,平衡常数不变 |

