��Ŀ����
��8��,ÿ��2�֣���ҵ����ȡCuCl2�������������£�
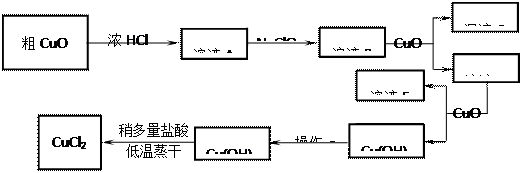
�����±����ݣ��ش��������⣺
����ҺA�м���NaClO��Ŀ���� ��
������ҺB�м���CuO�������� ��
�Dz���a��Ŀ���� ��
����Cu(OH)2��������ʹCu(OH)2ת��ΪCuCl2�����ö�������͵������ɵ�Ŀ���� ��

�����±����ݣ��ش��������⣺
| �� �� | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| �ܶȻ���25�� | 8.0��10��16 | 2.2��10��20 | 4.0��10��38 |
| ��ȫ����ʱ��pH��Χ | ��9.6 | ��6.4 | 3��4 |
������ҺB�м���CuO�������� ��
�Dz���a��Ŀ���� ��
����Cu(OH)2��������ʹCu(OH)2ת��ΪCuCl2�����ö�������͵������ɵ�Ŀ���� ��
�� ��Fe2������ΪFe3����ʹ���������ȫ
�Ƶ�����Һ��pHΪ3��4��ʹF e3����ȫת��ΪF
e3����ȫת��ΪF e(OH)3����������Fe3��
e(OH)3����������Fe3��
��ϴ��Cu(OH)2����Ŀ���������
������Cu2����ˮ��
�Ƶ�����Һ��pHΪ3��4��ʹF
 e3����ȫת��ΪF
e3����ȫת��ΪF e(OH)3����������Fe3��
e(OH)3����������Fe3����ϴ��Cu(OH)2����Ŀ���������
������Cu2����ˮ��
��

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
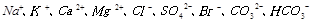 �����ӡ�
�����ӡ�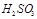 ��
��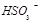 ��
��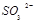 ����������д������һ����Ӧ�ķ���ʽ�� ��
����������д������һ����Ӧ�ķ���ʽ�� ��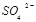 Ũ�����������������Ȼ��ˮ��ȣ�
Ũ�����������������Ȼ��ˮ��ȣ�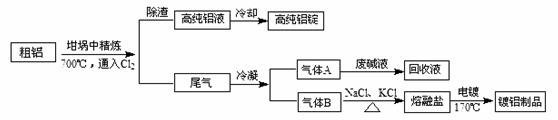
 ��NaCl�۵�Ϊ801�棻AlCl3��181��������
��NaCl�۵�Ϊ801�棻AlCl3��181��������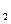 ����ֹ��Ⱦ�������������ԭ�ϣ����ŷ�ǰ�������β���������跨�����ۺ����á�
����ֹ��Ⱦ�������������ԭ�ϣ����ŷ�ǰ�������β���������跨�����ۺ����á� ��Һ���գ�Ȼ���ټ���������Һ��д�����������еĻ�ѧ��Ӧ����ʽ��
��Һ���գ�Ȼ���ټ���������Һ��д�����������еĻ�ѧ��Ӧ����ʽ��  �����·����봫ͳ������ȣ����ŵ��� ��
�����·����봫ͳ������ȣ����ŵ��� �� ( O
( O