题目内容
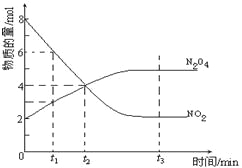
【题目】一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: molL﹣1s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率.
【答案】(1)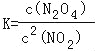 ;
;
(2)0.1;
(3)t3;
(4)>.
【解析】
试题分析:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol﹣3mol=1mol,根据v=![]() 计算v(N2O4);
计算v(N2O4);
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,据此结合图象判断;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行.
解:(1)可逆反应2NO2N2O4的平衡常数表达式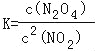 ,故答案为:
,故答案为: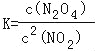 ;
;
(2)由图可知,从t1至t2时N2O4的物质的量变化量为4mol﹣3mol=1mol,故v(N2O4)=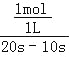 =0.1mol/(Ls),
=0.1mol/(Ls),
故答案为:0.1;
(3)到达平衡时,反应混合物各组分的物质的量不发生变化,由图象可知,t3时刻处于平衡状态,故答案为:t3;
(4)t1时刻后,NO2浓度降低,N2O4浓度增大,未到达平衡状态,反应向正反应进行,故正反应速率大于逆反应速率,
故答案为:>.

练习册系列答案
相关题目