题目内容
【题目】工业上用![]() 和氨水的混合液浸取废铜矿渣中的单质铜,得到
和氨水的混合液浸取废铜矿渣中的单质铜,得到![]() 。某小组同学欲通过实验探究其原理。
。某小组同学欲通过实验探究其原理。
(查阅资料)i.![]() 呈深蓝色,
呈深蓝色,![]() ;受热易分解,放出氨气。
;受热易分解,放出氨气。
ii.![]() 在水溶液中不稳定,
在水溶液中不稳定,![]() 在溶液中只能以
在溶液中只能以![]() 等络合离子的形式稳定存在;
等络合离子的形式稳定存在;![]() 无色,易被氧气氧化为
无色,易被氧气氧化为![]() 。
。
(实验1)制备![]() 。
。
向盛有![]() 溶液的试管中滴加
溶液的试管中滴加![]() 氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液。经分离得到
氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液。经分离得到![]() 晶体。
晶体。
(1)资料表明,向![]() 溶液中滴加氨水,可能会生成浅蓝色
溶液中滴加氨水,可能会生成浅蓝色![]() 沉淀。
沉淀。
①该小组同学取实验1中浅蓝色沉淀,洗涤后,____________(补全实验操作和现象),证明沉淀中含有![]() 。
。
②补全实验1中生成![]() 沉淀的离子方程式:
沉淀的离子方程式:
![]() ____________+
____________+![]() ____________
____________
(2)甲同学设计实验证明深蓝色溶液中含![]() :加热深蓝色溶液并检验逸出气体为氨气。你认为此方案____________(填“可行”或“不可行”),理由是____________。
:加热深蓝色溶液并检验逸出气体为氨气。你认为此方案____________(填“可行”或“不可行”),理由是____________。
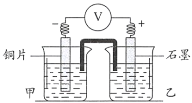
(实验2)探究用![]() 和氨水的混合液浸取单质铜得到
和氨水的混合液浸取单质铜得到![]() 的原理。
的原理。
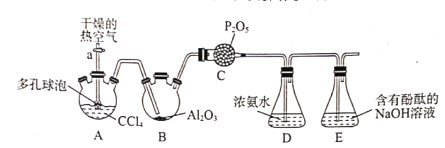
编号 | 实验装置及部分操作 | 烧杯中溶液 | 实验现象 |
2-1 |
实验开始,先读取电压表示数,后迅速将其换成电流表,继续实验, 10 min内记录甲烧杯中现象 | 甲: 乙: | 电压表指针迅速偏转至0.1V;甲中溶液无明显变化 |
2-2 | 甲: 乙: | 电压表指针迅速偏转至0.3V;甲中溶液无明显变化 | |
2-3 | 甲: 乙:溶液A | 电压表指针迅速偏转至0.35V;甲中溶液无明显变化 | |
2-4 | 甲: 乙: | 电压表指针迅速编转至0.65V;几分钟后,甲烧杯溶液逐渐由无色变蓝色 |
已知:其他条件相同时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,检测到的电压越大
(3)溶液A为____________。
(4)对比实验2-1和2-2,可以得到结论是____________。
(5)实验2-4中,甲烧杯中溶液由无色变为蓝色的原因是____________。
(6)依据上述实验,分析用![]() 和氨水的混合液浸取单质铜的原理:____________。
和氨水的混合液浸取单质铜的原理:____________。
【答案】先加入过量稀盐酸,再加入![]() 溶液,观察到有白色沉淀产生
溶液,观察到有白色沉淀产生 ![]()
![]() 不可行 实验1中氨水过量,过量的氨水受热分解也会产生氨气
不可行 实验1中氨水过量,过量的氨水受热分解也会产生氨气 ![]() 溶液 相同条件下,
溶液 相同条件下,![]() 的氧化性弱于
的氧化性弱于![]() 甲烧杯中发生电极反应:Cu-e-+2NH3=
甲烧杯中发生电极反应:Cu-e-+2NH3=![]() ,
,![]() 被空气中的氧气氧化为蓝色的
被空气中的氧气氧化为蓝色的![]()
![]() 将Cu氧化为
将Cu氧化为![]() ,氨水对浸取单质铜的反应有促进作用
,氨水对浸取单质铜的反应有促进作用
【解析】
本实验先合成了![]() ,通过原电池的装置探究制得
,通过原电池的装置探究制得![]() 的原理。原电池的负极发生氧化反应,负极材料为Cu,正极发生还原反应,正极区有
的原理。原电池的负极发生氧化反应,负极材料为Cu,正极发生还原反应,正极区有![]() ,有电压产生说明二者发生了反应,根据负极区溶液变蓝的现象,推断出负极区发生了
,有电压产生说明二者发生了反应,根据负极区溶液变蓝的现象,推断出负极区发生了![]() 被氧化为
被氧化为![]() 的反应,从而推断出负极区生成了
的反应,从而推断出负极区生成了![]() ,最终得出总反应是
,最终得出总反应是![]() 将Cu氧化为
将Cu氧化为![]() 。同时通过对照实验,得出氨水对浸取单质铜的反应有促进作用的结论。
。同时通过对照实验,得出氨水对浸取单质铜的反应有促进作用的结论。
(1)①检验SO42-时,先加入过量稀盐酸,排除Ag+、CO32-、SO32-等离子的干扰,再加入![]() 溶液,有白色的BaSO4沉淀产生;
溶液,有白色的BaSO4沉淀产生;
②根据题意,反应加的是氨水,故反应物中有NH3![]() H2O,根据元素守恒,NH3
H2O,根据元素守恒,NH3![]() H2O的系数需要配2,反应后产物中有2个NH4+生成;
H2O的系数需要配2,反应后产物中有2个NH4+生成;
(2)在制备![]() 时,加入的氨水过量,一水合氨受热后也会产生氨气,NH3·H2O
时,加入的氨水过量,一水合氨受热后也会产生氨气,NH3·H2O![]() NH3↑+H2O,所以不一定是
NH3↑+H2O,所以不一定是![]() 分解产生的氨气;
分解产生的氨气;
(3)实验2-1和2-2用![]() 和
和![]() 在没加氨水的情况下进行对照,实验2-3和2-4在加了氨水的情况下进行对照,因此溶液A为
在没加氨水的情况下进行对照,实验2-3和2-4在加了氨水的情况下进行对照,因此溶液A为![]() 溶液;
溶液;
(4)由表可知,实验2-1产生的电压差为0.1V,实验2-2产生的电压差为0.3V,根据其他条件相同时,参与原电池反应的氧化剂的氧化性越强,检测到的电压越大,所以![]() 的氧化性弱于
的氧化性弱于![]() ;
;
(5)甲烧杯中发生电极反应:Cu-e-+2NH3=![]() ,
,![]() 无色,但它易被氧气氧化为
无色,但它易被氧气氧化为![]() ,
,![]() 呈深蓝色,所以溶液变蓝是因为
呈深蓝色,所以溶液变蓝是因为![]() 被空气中的氧气氧化为
被空气中的氧气氧化为![]() ;
;
(6)首先根据原电池的总反应![]() +Cu=2
+Cu=2![]() ,说明
,说明![]() 可以将Cu氧化为
可以将Cu氧化为![]() ,再根据实验2-3、2-4与实验2-1、2-2的对比,加入氨水后,电压差明显增大,说明氨水对浸取单质铜的反应有促进作用;
,再根据实验2-3、2-4与实验2-1、2-2的对比,加入氨水后,电压差明显增大,说明氨水对浸取单质铜的反应有促进作用;

 作业辅导系列答案
作业辅导系列答案【题目】消除尾气中的NO是环境科学研究的热点课题。
I.NO氧化机理
已知:2NO(g)+O2(g) ![]() 2NO2(g)△H=-110kJ·mol-1
2NO2(g)△H=-110kJ·mol-1
25℃时,将NO和O2按物质的量之比为2:1充入恒容反应容器中,用测压法研究其反应的进行情况。体系的总压强p随时间t的变化如下表所示(忽略NO2与N2O4的转化)
t/min | 0 | 80 | 160 |
|
p/kPa | 75.0 | 63.0 | 55.0 | 55.0 |
(1)0~80min,v(O2)=_____kPa/min;随着反应进行,反应速率逐渐减小的原因是______________。
用平衡分压代替平衡浓度所得到的平衡常数用K(p)表示,25℃时,K(p)的值为_______(保留3位有效数字)。
(2)查阅资料,对于总反应2NOg)+O2(g) ![]() 2NO2(g)有如下两步历程
2NO2(g)有如下两步历程
第一步2NO(g) ![]() N2O2(g) 快速反应
N2O2(g) 快速反应
第二步N2O2(g)+O2(g) ![]() 2NO2(g) 慢反应
2NO2(g) 慢反应
总反应速率主要由第_____步决定;若利用分子捕获器适当减少反应容器中的N2O2,总反应的平衡常数K(p)将___(填“增大”、“减小”或“不变”);若提高反应温度至35℃,则体系压强P(35℃)______P(25℃)(填“大于”、“等于”或“小于”)。
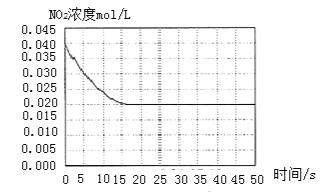
II. 某温度下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如上图所示。
(1)反应体系达平衡后压强为P1,若升高温度,再次达平衡后,混合气体的平均相对分子质量______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() ;
;
(2)若在恒温恒容条件下,向平衡体系中充入一定量O2,再次达平衡后,测得压强为P2,c(O2)=0.09mol/L,则P2:P1=______
(3)该温度下反应2NO(g)+O2(g) ![]() 2NO2(g)的化学平衡常数K为______。
2NO2(g)的化学平衡常数K为______。