题目内容
【题目】从镍钼矿渣(主要含有MoO3、NiO、MgO和Fe2O3)中提取元素,其主要工业流程如图:
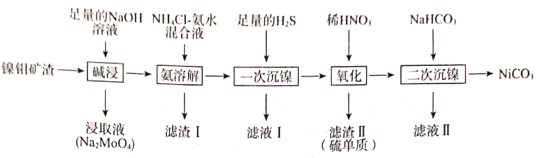
已知:①MoO3难溶于水,可溶于强碱溶液。
②Fe2O3、MgO不溶于NH4Cl—氨水混合液,NiO可溶于NH4Cl—氨水混合液生成[Ni(NH3)6]2+。
③已知部分金属离子形成氢氧化物沉淀的pH见下表:
pH(开始沉淀) | pH(完全沉淀) | |
Fe3+ | 1.52 | 3.18 |
Mg2+ | 8.10 | 9.43 |
请回答下列问题:
(1)“碱浸”时应先将镍钼矿渣粉碎,再与NaOH在80℃下反应2小时,该操作的目的为___。
(2)“碱浸”时,MoO3发生反应的离子方程式为___。
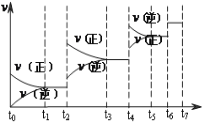
(3)“氨溶解”的目的为___,“氨溶解”过程中反应条件的选择性实验数据如图所示,“氨溶解”过程中需要控制温度在50~70℃之间,温度过高或过低都会导致产品的产量降低,请解释原因___。

(4)简述利用“滤渣I”制备纯净的铁红的方法:___。
(5)“一次沉镍”时加入H2S的目的是将镍元素转化为NiS沉淀,对应的离子方程式为___。
(6)“氧化”时发生反应的氧化剂与还原剂的物质的量之比为___。
(7)“二次沉镍”时,发生反应的离子方程式为___。
(8)已知:某温度时,Ksp(NiC2O4)=4.0×10-10,Ksp(NiCO3)=1.60×10-8。此温度下,将碳酸镍固体投入到1L一定浓度的Na2C2O4溶液中,若要一次性恰好将1molNiCO3完全转化成NiC2O4,则所需Na2C2O4溶液的浓度c(Na2C2O4)=___(忽略溶液体积的变化)。
【答案】加快反应速率,提高镍元素的浸出率 MoO3+2OH-=MoO42-+H2O 实现镍元素和铁、镁元素的分离 浓度过低NiO的浸出速率比较低,温度过高会导致氨的挥发,氯化按分解,氨水的利用率低 用稀硫酸溶解滤渣I,然后向反应后的溶液中加入碱凋节pH到3.18~8.10之间,过滤、洗涤、干燥后,经煅烧可制得铁红 [Ni(NH3)6]2++5H2S=NiS↓+6NH4++4HS- 2:3 Ni2++2HCO3-=NiCO3↓+H2O+CO2↑ 1.025molL-1
【解析】
镍钼矿渣(主要含有MoO3、NiO、MgO和Fe2O3)先加入足量的NaOH溶液,MoO3可溶于强碱,溶解得到Na2MoO4;滤渣主要含NiO、MgO和Fe2O3,再加入NH4Cl-氨水混合液,NiO溶解得到[Ni(NH3)6]2+,再过滤,滤渣I主要有MgO和Fe2O3;滤液中通入足量的硫化氢,和[Ni(NH3)6]2+反应得到NiS沉淀,过滤向沉淀中加入稀硝酸,S元素被氧化得到硫单质,之后向滤液中加入碳酸氢钠得到碳酸镍沉淀。
(1)将镍钼矿渣粉碎,固体表面积增大,目的是加快反应速率,提高镍元素的浸出率;
(2)根据题目所给信息可知MoO3可溶于强碱,溶解得到Na2MoO4,根据电荷守恒可得离子方程式为MoO3+2OH-=MoO42-+H2O;
(3)MgO和Fe2O3不溶于NH4Cl-氨水混合液,NiO溶于NH4Cl-氨水混合液生成[Ni(NH3)6]2+,所以“氨溶解”的目的是实现镍元素和铁、镁元素的分离;利用NH4Cl-氨水混合液“氨溶解”时,浓度过低NiO的浸出速率比较低,温度过高会导致氨的挥发,氯化铵分解,氨水的利用率低;
(4)根据分析可知滤渣I的主要成分为MgO和Fe2O3,需要制备Fe2O3,根据题目所给信息可知pH为3.18时Fe3+完全沉淀,而pH为8.10时Mg2+开始沉淀,所以可以通过调节镁离子和铁离子混合液的pH值实现二者的分离,具体操作为:用稀硫酸溶解滤渣I,然后向反应后的溶液中加入碱调节pH到3.18~8.10之间,过滤、洗涤、干燥后,经煅烧可制得铁红;
(5)“一次沉镍”时加入H2S的目的是将镍元素转化为NiS沉淀,H2S过量,所以最终产物中有HS-,根据元素守恒和电荷守恒可得离子方程式为[Ni(NH3)6]2++5H2S=NiS↓+6NH4++4HS-;
(6)氧化时稀硝酸被还原成NO,化合价降低3价,NiS被氧化成S,化合价升高2价,根据电子守恒可知氧化剂:还原剂=2:3;
(7)加入碳酸氢钠,得到碳酸镍沉淀,说明碳酸氢根电离出的碳酸根和镍离子生成沉淀,促进碳酸氢根的电离,产生大量氢离子,氢离子和碳酸氢根结合又生成二氧化碳,据此可知离子方程式为Ni2++2HCO3-=NiCO3↓+H2O+CO2↑;
(8)NiCO3转化成NiC2O4的离子方程式为NiCO3(s)+C2O42-![]() NiC2O4(s)+CO32-,该反应的平衡常数K=
NiC2O4(s)+CO32-,该反应的平衡常数K=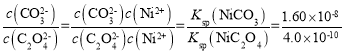 =40,处理后的溶液中碳酸根的浓度为1mol/L,则溶液中草酸根的浓度为0.025mol/L,沉淀NiC2O4中含有1mol草酸根,所以加入的草酸钠溶液的浓度c(Na2C2O4)=1.025mol/L。
=40,处理后的溶液中碳酸根的浓度为1mol/L,则溶液中草酸根的浓度为0.025mol/L,沉淀NiC2O4中含有1mol草酸根,所以加入的草酸钠溶液的浓度c(Na2C2O4)=1.025mol/L。