题目内容
【题目】下列说法正确的是
A.反应C(s)+H2O(g)![]() CO(g)+H2(g)达平衡后,加入单质碳平衡必定向正反应方向移动
CO(g)+H2(g)达平衡后,加入单质碳平衡必定向正反应方向移动
B.A2(g)+3B2(g)![]() 2AB3(g)达平衡后,若保待容器压强不变,继续通入0.2mol A2和0.6mol B2,平衡向正反应方向移动,则A2的转化率一定变大
2AB3(g)达平衡后,若保待容器压强不变,继续通入0.2mol A2和0.6mol B2,平衡向正反应方向移动,则A2的转化率一定变大
C.2RO2(g)+O2(g)![]() 2RO3(g) △H=-197kJ·mol-1,升高温度,正反应速率减小
2RO3(g) △H=-197kJ·mol-1,升高温度,正反应速率减小
D.在一定温度下,一定容积的密闭容器中发生反应:C(s)+H2O(g)![]() H2(g)+CO(g),当混合气体的相对平均分子质量不再发生变化时,反应达到平衡
H2(g)+CO(g),当混合气体的相对平均分子质量不再发生变化时,反应达到平衡
【答案】D
【解析】
A. 单质碳为固体,对化学反应速率没有影响,A项错误;
B. A2(g)+3B2(g)![]() 2AB3(g)达平衡后,若保待容器压强不变,继续通入0.2mol A2和0.6mol B2,物质的量与体积成正比,可能浓度不变,则平衡不移动,即A2的转化率不变,B项错误;
2AB3(g)达平衡后,若保待容器压强不变,继续通入0.2mol A2和0.6mol B2,物质的量与体积成正比,可能浓度不变,则平衡不移动,即A2的转化率不变,B项错误;
C. 化学反应速率与反应的热效应无关,与活化分子百分数有关,升高温度,正反应速率一定增大,C项错误;
D. 当混合气体的平均相对分子质量为气体的总质量与气体的总的物质的量的比值,反应C(s)+H2O(g)![]() H2(g)+CO(g)假设开始有 1mol H2O(g)参与,则起始气体的平均相对分子质量为18,假设全部转化为氢气和一氧化碳,则得到的混合气体的相对分子质量为2+28=30,则说明随着反应的进行,气体的平均相对分子质量为变量,故当混合气体的相对平均分子质量不再发生变化时,反应达到平衡,D项正确;
H2(g)+CO(g)假设开始有 1mol H2O(g)参与,则起始气体的平均相对分子质量为18,假设全部转化为氢气和一氧化碳,则得到的混合气体的相对分子质量为2+28=30,则说明随着反应的进行,气体的平均相对分子质量为变量,故当混合气体的相对平均分子质量不再发生变化时,反应达到平衡,D项正确;
答案选D。

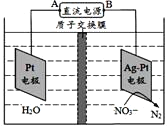
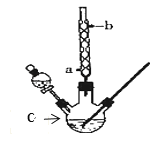
【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去)。已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
请回答下列问题:
(1)仪器C的名称为______,球形冷凝管的作用是_____。
(2)向C中加入反应物,待充分反应后,将C中的混合物倒入装有饱和碳酸钠溶液的烧杯中充分振荡洗涤。饱和碳酸钠溶液作用是(填字母):_____
A.中和乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(3)经多次振荡洗涤、静置分液后,为了进一步提纯乙酸乙酯,可采用蒸馏的方法,蒸馏时控制温度在__左右,温度计的水银球应位于____。
(4)若实验所用乙酸质量为2.4g,乙醇质量为2.1g,得到纯净的产品质量为2.64g,则乙酸乙酯的产率是______。
(5)乙酸乙酯与氢氧化钠溶液发生反应的化学方程式为____________。
【题目】测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等