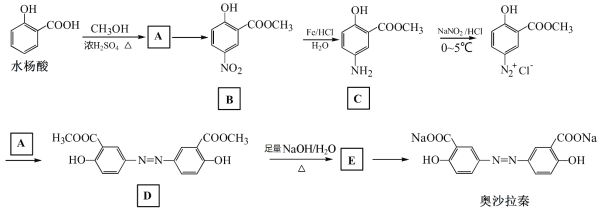
题目内容
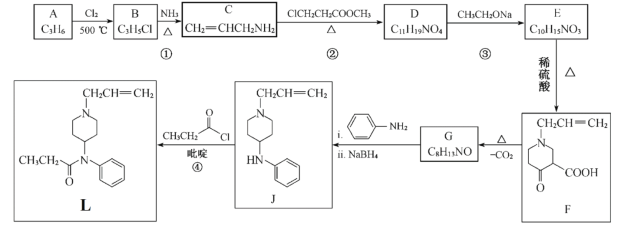
【题目】芬太尼类似物L具有镇痛作用。它的合成方法如下:
已知:
I、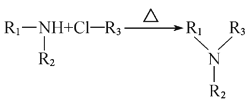 +HCl
+HCl
II、![]()
![]()
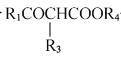 +R2OH;
+R2OH;
III、 (
(![]() 为氢或烃基)
为氢或烃基)
回答下列问题:
(1)A是一种烯烃,化学名称为______,其分子中最多有__________个原子共面。
(2) B中官能团的名称为_____、_____。②的反应类型为________
(3)③的化学方程式为________
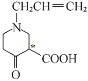
(4)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。指出F的结构简式中手性碳原子并用星号(*)标出F中的手性碳________。G的结构简式为________。
(5)已知④有一定的反应限度,反应进行时加入吡啶(一种有机碱),其作用是________。
(6)参照上述合成路线,写出以环已烯(![]() )和乙醇为起始原料经三步制备化合物
)和乙醇为起始原料经三步制备化合物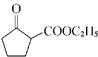 的合成路线________。
的合成路线________。
(已知:![]() 其他试剂任选)
其他试剂任选)
【答案】丙烯 7 碳碳双键 氯原子 取代反应 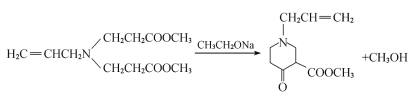
 吸收反应生成的HCl 提高反应转化率
吸收反应生成的HCl 提高反应转化率 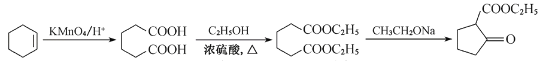
【解析】
由A、B的分子式,C的结构简式,可知A为CH3CH=CH2,A发生取代反应生成B为ClCH2CH=CH2。反应①为取代反应。由C、D的分子式,可知反应②发生信息I中取代反应,可知D为 。由信息II中取代反应、结合E的分子式,可知E为
。由信息II中取代反应、结合E的分子式,可知E为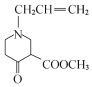 。E发生酯的水解反应生成F。对比F、J的结构简式,可知F脱羧生成G,G与苯胺脱去1分子水生成J,故G为
。E发生酯的水解反应生成F。对比F、J的结构简式,可知F脱羧生成G,G与苯胺脱去1分子水生成J,故G为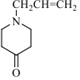 。J与
。J与![]() 发生取代反应生成L;
发生取代反应生成L;
(6)由信息II可知,由![]() 反应得到
反应得到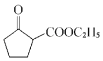 ;
;![]() 用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到
用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到![]() 。
。
(1)A属于烯烃,A的结构简式为CH2=CH﹣CH3,A名称为:丙烯,旋转碳碳单键可以使甲基中1个H原子处于碳碳双键的平面结构内,分子中最多有7个原子共面;
(2)B为ClCH2CH=CH2,B中官能团有碳碳双键、氯原子,反应②是B的氨基中氢原子被﹣CH2CH2COOCH3替代,属于取代反应;
(3)反应③的化学方程式为: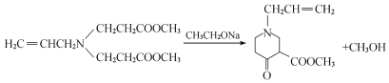 ;
;
(4)F的结构简式为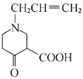 ,用星号(*)标出F中的手性碳原子为:
,用星号(*)标出F中的手性碳原子为: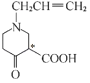 ,G的结构简式为:
,G的结构简式为: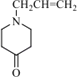 ;
;
(5)反应④为取代反应,生成有机物的同时可生成HCl,而吡啶呈碱性,可与HCl发生中和反应,使平衡正向移动,提高J的产率;
(6)由信息II可知,由![]() 反应得到
反应得到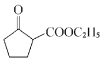 。
。![]() 用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到
用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到![]() ,合成路线流程图为:
,合成路线流程图为: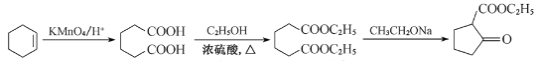 。
。

【题目】I.能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应 I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
反应 II:CO(g)+2H2(g) ![]() CH3OH(g) △H2
CH3OH(g) △H2
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断△H2____0(填“>”、“<”或“=”)
②若容器容积不变,下列措施可增加甲醇产率的是____
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用合适的催化剂 D.充入He,使体系总压强增大
E.按原比例再充入CO和H2
③某温度下,将2molCO和6molH2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO) =0.2mol/L,则CO的转化率为______,此时的温度为___(从上表中选择);
④恒温下,1 molCO和nmolH2在一个容积可变的密闭容器中反应达到平衡后,生成 amolCH3OH。若起始时放入3molCO、3nmolH2,则达平衡时生成CH3OH_______mol。
II.25℃时,电离平衡常数:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(1)下列四种离子结合质子的能力由大到小的顺序是__________;(填编号)
A.CO32- B.ClO- C.CH3COO- D.HCO3-
(2)下列反应不能发生的是:________
A.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
B.ClO-+CH3COOH=CH3COO-+HClO
C.CO32-+HClO=CO2↑ +H2O +ClO-
D.2ClO-+CO2
(3)用蒸馏水稀释0.10 mol/L的醋酸,则下列各式表示的数值随水量的增加而增大的是_____;
A. B.
B. C.
C.![]() D.
D.
(4)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程 pH 变化如图,则HX的电离平衡常数_______(填“大于”、“等于”或“小于”)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)______醋酸溶液中水电离出来的 c(H+)(填“大于”、“等于”或“小于”)

III.以CH3OH燃料电池为电源电解法制取ClO2。二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH_____(填“增大”、“减小”或“不变”),负极反应式为________。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。阳极产生ClO2的反应式为_________。

③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_________mol。
④在阴极室中加入少量的NaOH的作用是__________。