题目内容
15.中和热是在稀溶液中,强酸、强碱发生中和反应生成1mol水时放出的热量,中和热为57.3kJ/mol.下列热化学方程式中正确的是( )| A. | HNO3(aq)+KOH(aq)═H2O(l)+KNO3(aq)△H>-57.3 kJ/mol | |
| B. | HNO3(aq)+NH3•H2O(aq)═H2O(l)+NH4NO3(aq)△H<-57.3 kJ/mol | |
| C. | CH3COOH(aq)+KOH(aq)═H2O(l)+CH3COOK(aq)△H<-57.3 kJ/mol | |
| D. | CH3COOH(aq)+NH3•H2O(aq)═H2O(l)+CH3COONH4(aq)△H>-57.3 kJ/mol |
分析 中和热是在稀溶液中,强酸、强碱发生中和反应生成1mol水时放出的热量,应注意的是:①稀的酸和碱溶液,如果是浓硫酸,在和碱反应时被稀释放热;②强酸和强碱,如果是弱酸,电离吸热;③衡量标准是生成1mol水.据此分析.
解答 解:A、HNO3和 KOH分别是强酸和强碱,当其反应生成1mol水时,放出的热量即为57.3kJ/mol,故反应热△H应等于-57.3 kJ/mol,故A错误;
B、NH3•H2O是弱碱,电离吸热,故当NH3•H2O与HNO3生成1mol水时,放出的热量小于57.3 kJ,则反应热△H应大于-57.3 kJ/mol,故B错误;
C、CH3COOH是弱酸,电离吸热,故当CH3COOH与KOH生成1mol水时,放出的热量小于57.3 kJ,则反应热△H应大于-57.3 kJ/mol,故C错误;
D、NH3•H2O是弱碱,CH3COOH是弱酸,电离吸热,故当CH3COOH与NH3•H2O生成1mol水时,放出的热量小于57.3 kJ,则反应热△H应大于-57.3 kJ/mol,故D正确.
故选D.
点评 本题考查了中和热的热化学方程式的书写,应注意的是弱电解质电离吸热,对反应热有影响,难度不大.

练习册系列答案
相关题目
1.C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2.将1.20g C跟16.0g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12L气体(标准状况),生成沉淀的质量为5.00g.下列说法正确的是( )
| A. | 反应后的固体混合物中还含有碳 | |
| B. | 反应后的固体混合物总质量为12.8 g | |
| C. | 反应后的固体混合物中氧化物的物质的量为0.05 mol | |
| D. | 反应后的固体混合物中单质Cu的质量为12.8 g |
6.下列叙述中,正确的是( )
| A. | 可用带玻璃塞的玻璃瓶盛放NaOH溶液 | |
| B. | SiO2和CO2都是酸性氧化物,既能与水反应,又能与NaOH溶液反应 | |
| C. | SiO2与纯碱在高温条件下反应生成CO2,说明硅酸的酸性比碳酸强 | |
| D. | 石灰石是工业制备普通玻璃和普通水泥的共同原料 |
3.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 大量使用化肥和农药,以提高农作物产量 | |
| C. | 不随意丢弃旧电池,生活垃圾分类放置 | |
| D. | “绿色化学”的核心是使原料尽可能全部转化为目标产物 |
10.如图是元素周期表的一部分,下列说法正确的是( )
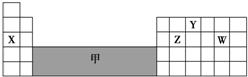

| A. | 可在灰色区域“甲”中寻找半导体材料 | |
| B. | X、Z、W 最高价氧化物对应的水化物之间两两能相互反应 | |
| C. | 气态氢化物的稳定性:Z<W | |
| D. | X只能形成一种氧化物 |
20.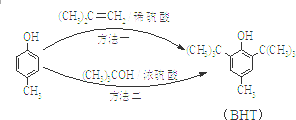 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从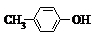 出发合成BHT的方法有如下两种.下列说法不正确的是( )
出发合成BHT的方法有如下两种.下列说法不正确的是( )
 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种.下列说法不正确的是( )
出发合成BHT的方法有如下两种.下列说法不正确的是( )| A. | 推测BHT在水中的溶解度小于苯酚 | |
| B. | BHT与 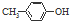 都能使酸性KMnO4褪色 都能使酸性KMnO4褪色 | |
| C. | 方法一和方法二的反应类型都是加成反应 | |
| D. | BHT与 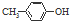 具有完全相同的官能团 具有完全相同的官能团 |
7.下列说法一定正确的是( )
| A. | CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 | |
| B. | 需要加热方能发生的反应一定是吸热反应 | |
| C. | 若反应X+Y=M是放热反应,该反应一定不用加热 | |
| D. | 硫酸与氢氧化钠发生中和反应生成水是放热反应,则水的能量比硫酸的能量低 |
4.X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期.X原子的最外层电子数是其电子层数的3倍.Z原子的核外电子数比Y原子少1.下列说法正确的是( )
| A. | 元素非金属性由强到弱的顺序是:X>Y>Z | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H4YO4 | |
| C. | 3种元素的气态氢化物中,Z的气态氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为 Z>Y>X |
5.下列各组有机物中,无论以何种比例混合,只要二者物质的量之和不变,完全燃烧时消耗氧气的物质的量和生成水的物质的量分别相等的是( )
| A. | 乙烷和乙醇 | B. | 乙烯和环丙烷 | C. | 苯和苯甲酸 | D. | 甲醛和甲酸 |