题目内容
7.下列说法一定正确的是( )| A. | CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 | |
| B. | 需要加热方能发生的反应一定是吸热反应 | |
| C. | 若反应X+Y=M是放热反应,该反应一定不用加热 | |
| D. | 硫酸与氢氧化钠发生中和反应生成水是放热反应,则水的能量比硫酸的能量低 |
分析 A、CO2与CaO的化合与CaCO3的分解是相反的过程;
B、反应条件与反应吸放热无必然的关系;
C、有些放热反应也需加热才能发生;
D、放热反应是反应物的总能量大于生成物的总能量.
解答 解:A、CO2与CaO的化合与CaCO3的分解是相反的过程,故CO2与CaO反应放热,则CaCO3的分解吸热,故A正确;
B、反应条件与反应吸放热无必然的关系,不能根据反应条件来判断反应吸放热,故B错误;
C、有些放热反应也需加热才能发生,如煤炭的燃烧需先加热才能进行,故C错误;
D、放热反应是反应物的总能量大于生成物的总能量,硫酸与氢氧化钠发生中和反应生成水是放热反应,只能说明1mol硫酸和2mol氢氧化钠的能量和大于2mol水和1mol硫酸钠的能量和,故D错误.
故选A.
点评 本题考查了反应吸放热与反应条件的关系,应注意的是反应条件与反应吸放热无必然的关系,不能根据反应条件来判断反应吸放热.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列说法不正确的是( )
| A. | Al箔插入稀HNO3中无现象因Al箔表面被HNO3氧化,形成致密的氧化膜 | |
| B. | “硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触 | |
| C. | “中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,必须干燥或润洗后方可使用 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
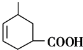
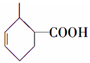
18.某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
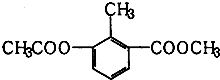

| A. | 一个分子中含有12个H原子 | B. | 该物质属于芳香族化合物 | ||
| C. | 能使酸性KMnO4溶液褪色 | D. | 苯环上的一氯代物有2种 |
15.中和热是在稀溶液中,强酸、强碱发生中和反应生成1mol水时放出的热量,中和热为57.3kJ/mol.下列热化学方程式中正确的是( )
| A. | HNO3(aq)+KOH(aq)═H2O(l)+KNO3(aq)△H>-57.3 kJ/mol | |
| B. | HNO3(aq)+NH3•H2O(aq)═H2O(l)+NH4NO3(aq)△H<-57.3 kJ/mol | |
| C. | CH3COOH(aq)+KOH(aq)═H2O(l)+CH3COOK(aq)△H<-57.3 kJ/mol | |
| D. | CH3COOH(aq)+NH3•H2O(aq)═H2O(l)+CH3COONH4(aq)△H>-57.3 kJ/mol |
19.${\;}_{6}^{13}$C-NMR(核磁共振)可以用于含碳化合物的结构分析,${\;}_{6}^{13}$C表示的碳原子( )
| A. | 核外有13个电子,其中6个能参与成键 | |
| B. | 核内有6个质子,核外有7个电子 | |
| C. | 质量数为13,原子序数为6,核内有7个质子 | |
| D. | 质量数为13,原子序数为6,核内有7个中子 |
16.铜~锌原电池如图所示,电解质溶液为稀硫酸,下列说法不正确的是( )
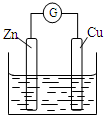

| A. | 铜电极上发生还原反应 | B. | 锌电极是原电池的负极 | ||
| C. | 电子从铜极经过外电路流向锌极 | D. | 锌电极上的反应为Zn-2e-═Zn2+ |
17.根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,判断下列说法正确的是( )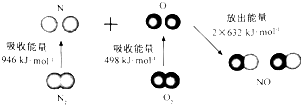

| A. | 该反应中反应物所具有的总能量高于生成物所具有的总能量 | |
| B. | 2 mol N原子结合生成N2(g)时需要放出946 kJ能量 | |
| C. | 1 mol NO(g)分子中的化学键断裂时需要放出632 kJ能量 | |
| D. | 该反应的热化学方程式为:N2+O2═2NO△H=+180 kJ/mol. |
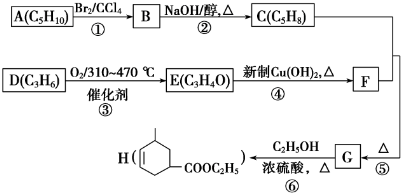
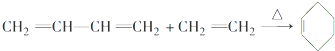
 .
. .
. .
. ;物质⑤的结构式O=C=O.
;物质⑤的结构式O=C=O.