题目内容
下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目 的 | 分离方法 | 原 理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D | 除去丁醇中的乙醇 | 蒸馏 | 丁醇与乙醇的沸点相差较大 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:实验评价题
分析:A.乙醇与水混溶,不分层;
B.乙酸乙酯和乙醇不分层;
C.NaCl的溶解度受温度影响不大,而硝酸钾的溶解度受温度影响大;
D.丁醇与乙醇的沸点不同,且差异较大.
B.乙酸乙酯和乙醇不分层;
C.NaCl的溶解度受温度影响不大,而硝酸钾的溶解度受温度影响大;
D.丁醇与乙醇的沸点不同,且差异较大.
解答:
解:A.乙醇与水混溶,不分层,不能利用乙醇作萃取剂,应选苯或四氯化碳等,故A错误;
B.乙酸乙酯和乙醇不分层,不能利用分液法分离,故B错误;
C.NaCl的溶解度受温度影响不大,而硝酸钾的溶解度受温度影响大,则利用重结晶分离,原理解释不合理,故C错误;
D.丁醇与乙醇的沸点不同,且差异较大,则蒸馏可除去丁醇中的乙醇,故D正确;
故选D.
B.乙酸乙酯和乙醇不分层,不能利用分液法分离,故B错误;
C.NaCl的溶解度受温度影响不大,而硝酸钾的溶解度受温度影响大,则利用重结晶分离,原理解释不合理,故C错误;
D.丁醇与乙醇的沸点不同,且差异较大,则蒸馏可除去丁醇中的乙醇,故D正确;
故选D.
点评:本题考查物质分离提纯方法的选择和应用,为高频考点,把握物质的性质及性质差异为解答的关键,注意常见混合物分离提纯的方法,题目难度不大.

练习册系列答案
相关题目
验证汽油是混合物的方法是( )
| A、测量密度 | B、测沸点 |
| C、将汽油点燃 | D、闻气味 |
常温下,将a mL b mol/L CH3COOH溶液加入到c mL d mol/L NaOH溶液中.下列结论中,不正确的是( )
| A、如果ab=cd,则反应后溶液的pH>7 |
| B、如果a=c,且反应后溶液的pH<7,则b<d |
| C、如果a=c、b=d,则反应后的溶液中c(CH3COO-)<c(Na+) |
| D、如果反应后溶液的pH=7,则此溶液中c(CH3COO-)=c(Na+) |
下列反应的离子方程式不正确的是( )
| A、向漂白粉中通人少量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | ||||
| B、将CO2通入到纯碱饱和溶液中:2Na++CO32-+CO2+H2O═2NaHCO3↓ | ||||
| C、向Ba(OH)2溶液中加入足量的NaHCO3溶液:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O | ||||
D、将饱和FeCl3溶液滴入沸水中制胶体:Fe3++3H2O
|
常温下,下列各溶液的叙述中正确的是( )
| A、已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,c(Na+)-c(F-)<c(K+)-c(CH3COO-) |
| B、0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b |
| C、相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ |
| D、氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):C(SO42-)=1:1 |
下列除去杂质的方法错误的是( )
| A、除去SiO2中少量NH4Cl:在空气中充分灼烧 |
| B、除去铜器表面的铜绿[Cu2(OH)2CO3]:用盐酸浸泡,再用清水冲洗 |
| C、除去CO2中混有的少量的HCl:用NaOH溶液洗气,再干燥 |
| D、除去FeCl2溶液中混有的CuCl2:可在溶液中加入铁粉,充分反应后过滤 |
某烯烃的结构简式为:

其命名正确的是( )

其命名正确的是( )
| A、2-甲基-5-乙基-3,5己二烯 |
| B、2-乙基-1,3-己二烯 |
| C、6-甲基-3,4-庚二烯 |
| D、5-甲基-2-乙基-1,3-己二烯 |
下列说法中,正确的是( )
| A、相邻的原子之间的相互作用叫做化学键 |
| B、金属和非金属元素的相互化合,都能形成离子键 |
| C、非金属元素的原子半径比其离子半径小(氢除外),金属元素的原子的原子半径比其离子半径大 |
| D、甲元素原子半径比乙元素原子半径大,则甲的离子半径一定比乙的原子半径大 |
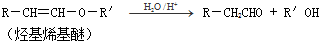
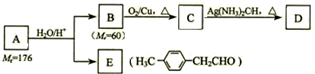
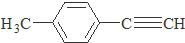 )的一条路线如下:
)的一条路线如下: