题目内容
下列反应的离子方程式不正确的是( )
| A、向漂白粉中通人少量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | ||||
| B、将CO2通入到纯碱饱和溶液中:2Na++CO32-+CO2+H2O═2NaHCO3↓ | ||||
| C、向Ba(OH)2溶液中加入足量的NaHCO3溶液:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O | ||||
D、将饱和FeCl3溶液滴入沸水中制胶体:Fe3++3H2O
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化硫具有还原性,能被次氯酸根氧化;
B.碳酸氢钠的溶解度小于碳酸钠;
C.向Ba(OH)2溶液中加入足量的NaHCO3溶液,二者按照1:2反应生成碳酸钡、碳酸钠和水;
D.三价铁离子为弱碱阳离子,水解生成氢氧化铁.
B.碳酸氢钠的溶解度小于碳酸钠;
C.向Ba(OH)2溶液中加入足量的NaHCO3溶液,二者按照1:2反应生成碳酸钡、碳酸钠和水;
D.三价铁离子为弱碱阳离子,水解生成氢氧化铁.
解答:
解:A.向漂白粉中通人少量的SO2气体,离子方程式为:SO2 +H2O+Ca2++ClO-=CaSO4 +2H++Cl-,故A错误;
B.将CO2通入到纯碱饱和溶液中,离子方程式为:2Na++CO32-+CO2+H2O═2NaHCO3↓,故B正确;
C.向Ba(OH)2溶液中加入足量的NaHCO3溶液,离子方程式为:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O,故C正确;
D.将饱和FeCl3溶液滴入沸水中制胶体:Fe3++3H2O
Fe(OH)3(胶体)+3H+,故D正确;
故选:A.
B.将CO2通入到纯碱饱和溶液中,离子方程式为:2Na++CO32-+CO2+H2O═2NaHCO3↓,故B正确;
C.向Ba(OH)2溶液中加入足量的NaHCO3溶液,离子方程式为:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O,故C正确;
D.将饱和FeCl3溶液滴入沸水中制胶体:Fe3++3H2O
| ||
故选:A.
点评:本题考查了离子方程式的书写,题目难度不大,明确化学反应的实质是解题关键,注意B选项中碳酸氢钠溶解度小于碳酸钠.

练习册系列答案
相关题目
某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为( )
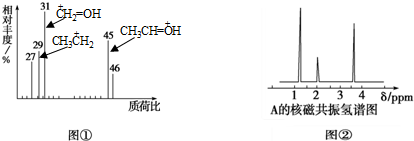

| A、HCOOH |
| B、CH3CHO |
| C、CH3CH2OH |
| D、CH3CH2CH2COOH |
化学与环境保护密切相关,下列叙述正确的是( )
| A、绿色化学的核心是应用化学原理治理环境污染 |
| B、处理废水时加人明矶作为消毒剂可以除去水中的杂质 |
| C、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的C02 |
| D、PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 |
常温下,pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化).下列说法正确的是( )
| A、原醋酸物质的量浓度大于0.01mol?L-1 |
| B、两种反应物中水电离出的c(H+)都是1×10-12mol?L-1 |
| C、反应后的溶液中:c(CH3COO-)+c(CH3COOH)=0.01mol?L-1 |
| D、反应后的溶液中:c(CH3COO-)=c(Na+)>c(H+)=c( OH-) |
将一定量的Fe2(SO4)3与(NH4)2Fe(SO4)2的混合物溶于水,配成2L溶液其中c(NH4+)=1mol/L,c(SO42-)=3mol/L,向此溶液中投入过量的铁粉后亚铁离子的浓度为(忽略水解)( )
| A、1.5mol/L |
| B、2mol/L |
| C、2.5mol/L |
| D、3mol/L |
关于银镜反应实验的下列说法中,正确的是( )
| A、做银镜反应的试管必须洁净,可以用碱液煮沸试管 |
| B、银氨溶液要可以现用现配,也可以久置再用 |
| C、银氨溶液的有效成分是氢氧化二氨合银[Ag(NH3)2OH] |
| D、银镜反应可以在酒精灯火焰上直接加热 |
对羟基苯甲醛(结构简式如图)是医药工业和香料工业的重要中间体.下列说法不正确的是( )
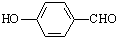

| A、能发生水解反应 |
| B、有两种含氧官能团 |
C、与苯甲酸(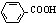 )互为同分异构体 )互为同分异构体 |
| D、一定条件下能与溴水、FeCl3溶液及银氨溶液反应 |