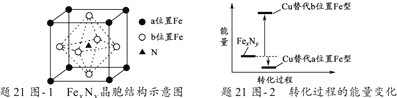
��Ŀ����
����Ŀ��x��y��z��w��nΪ���ֶ�����Ԫ�أ�����YԪ��ԭ�Ӻ�������������������Ӳ�����3�������������ڱ��е����λ����ͼ��ʾ��
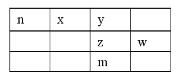
��ش��������⣺
(1)wλ�����ڱ��е�__________���ڣ���__________�塣
(2)n��z��w������Ԫ�����������ˮ���������������ǿ��˳��Ϊ��__________���û�ѧʽ��ʾ����
(3)������ʵ��˵��yԪ�صķǽ����Ա�zԪ�صķǽ�����ǿ����____
A��y������z����̬�⻯��ˮ��Һ��Ӧ����Һ�����
B����������ԭ��Ӧ�У�1moly���ʱ�1molz�õ��Ӷ�
C��y��z��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
D��yԪ�����������ˮ�������Ա�zԪ�����������ˮ��������ǿ
(4)y����Ԫ���γɵ�10�������г���![]() ��������Ϊ__________���ѧʽ����z����Ԫ���γɵ�18�������г���
��������Ϊ__________���ѧʽ����z����Ԫ���γɵ�18�������г���![]() �������ӵĵ���ʽΪ__________��
�������ӵĵ���ʽΪ__________��
(5)������nyz��������Ȼ���У�������NaOH��Һϴ�ӳ�ȥ��������nyz�ĵ���ʽΪ__________������NaOH��Һ��Ӧ���������������⣬����ˮ���ɣ��仯ѧ����ʽΪ__________��
(6)mԪ�ص�ԭ������Ϊ__________������һ��__________�������������������ǽ�������
���𰸡��� ��A ![]() AC
AC ![]()
![]()
![]()
![]() 34 �ǽ���
34 �ǽ���
��������
��Ԫ�����ڱ��ṹ��֪��yΪ�ڶ�����Ԫ�أ���yԪ��ԭ�Ӻ�������������������Ӳ�����3������yΪOԪ�أ��ɴ˿��Ƴ�nΪ̼Ԫ�أ�xΪ��Ԫ�أ�zΪ��Ԫ�أ�wΪ��Ԫ�أ��Դ˽����⣻
��1��wΪ��Ԫ�أ���ԭ������Ϊ17������3�����Ӳ㣬����㺬��7�����ӣ�λ�����ڱ��е������ڣ��ڢ�A�壬
�ʴ�Ϊ��������A��
(2)��Ԫ�������ɿ�֪��̼����������Ԫ�صķǽ�����ǿ��˳��ΪCl>S>C����������Ԫ�����������ˮ���������������ǿ��˳��ΪH2CO3<H2SO4<HClO4��
�ʴ�Ϊ��H2CO3<H2SO4<HClO4��
(3)A.������H2S��Һ��Ӧ����Һ����ǣ�˵�������������Ա���ǿ����˵����Ԫ�صķǽ����Ա�SԪ�صķǽ�����ǿ����A��ȷ��
B.��������ԭ��Ӧ�У�1mol������1molS�õ��Ӷ࣬������ǿ�����ʧ������û�б�Ȼ��ϵ����B����
C.Ԫ�صķǽ�����Խǿ���⻯����ȶ���Խǿ��O��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸߣ�˵�����ķǽ����Խ�ǿ����C��ȷ��
D.��Ԫ�ز�����������ۣ���ͨ����Ԫ�����������ˮ��������Ԫ�����������ˮ���������ǿ���Ƚ����ж���Ԫ�صķǽ����Ա���ǿ����D����
�ʴ�Ϊ��AC��
(4)��Ԫ�غ���Ԫ���γɵ�10�������г���+1��������ΪH3O+����Ԫ�غ���Ԫ���γɵ�18�������г���-1��������HS-�������ʽΪ![]() ��
��
�ʴ�Ϊ��H3O+��![]() ��
��
(5)�ʻ�������������̼���ӽṹ���ƣ���Ϊֱ���ͣ������ʽΪ![]() ��COS��NaOH��Һ��Ӧ���������������⣬����ˮ�������仯ѧ����ʽΪCOS+4NaOH=Na2CO3+Na2S+2H2O��
��COS��NaOH��Һ��Ӧ���������������⣬����ˮ�������仯ѧ����ʽΪCOS+4NaOH=Na2CO3+Na2S+2H2O��
�ʴ�Ϊ��![]() ��COS+4NaOH=Na2CO3+Na2S+2H2O��
��COS+4NaOH=Na2CO3+Na2S+2H2O��
(6)mԪ�غ�O��S����ͬһ���壬ΪSeԪ����ԭ��������S��18��Ϊ34������ͬһ������ϵ���Ԫ�����ʵݱ����֪��Ϊ�ǽ�����
�ʴ�Ϊ��34���ǽ�����

����Ŀ��Na2SO3��һ����Ҫ�Ļ�ԭ����I2O5��һ����Ҫ�������������߶��ǻ�ѧʵ�����е���Ҫ�Լ���
(1)��֪:2Na2SO3 (aq)+O2(aq)==2Na2SO4(aq) ��H =m kJ��mol-1��O2(g)![]() O2(aq) ��H =n kJ��mol-1 ����Na2SO3��Һ��O2(g)��Ӧ���Ȼ�ѧ����ʽΪ______________________________��
O2(aq) ��H =n kJ��mol-1 ����Na2SO3��Һ��O2(g)��Ӧ���Ȼ�ѧ����ʽΪ______________________________��
(2)Na2SO3�������ָ�������ƶ���������Σ�ƶ�������ʷ���Ϊv=k��ca(SO32-)��cb(O2)��kΪ������
�ٵ��ܽ���Ũ��Ϊ4.0 mg/L(��ʱNa2SO3������λ��ƶ����)ʱ��c(SO32-)��������ֵ��ϵ���±���ʾ����a=____��
c(SO32-)��103 | 3.65 | 5.65 | 7.65 | 11.65 |
V��106 | 10.2 | 24.4 | 44.7 | 103.6 |
�������ε����ʷ��̺Ͳ�ͬ�¶ȵ����ʳ���֮�����±���ʾ����֪1n(k2/k1)=Ea/R(1/T2-1/T1)��R Ϊ��������Ea(������)______(�>����<��)Ea(ƶ����)��
��Ӧ�� | ���ʷ��� | k(297.0K)/k(291.5K) |
������ | v= k��c(SO32-)��c(O2) | 1.47 |
ƶ���� | v= k��ca(SO32-)��cb(O2) | 2.59 |
(3)�����ʵ�����Na2SO3��Na2SO4�����Һ�У�c(SO32-) +c( HSO3-)______(�>����<����=��)c(SO42-)��
(4)����I2O5������CO ��Ⱦ���䷴ӦΪI2O5(s)+5CO(g) ![]() 5CO2(g)+I2(s)����ͬ�¶��£���װ������I2O5�����2 L �����ܱ�������ͨ��2 mol CO�����CO2��������������(CO2) ��ʱ��t�ı仯������ͼ��ʾ��
5CO2(g)+I2(s)����ͬ�¶��£���װ������I2O5�����2 L �����ܱ�������ͨ��2 mol CO�����CO2��������������(CO2) ��ʱ��t�ı仯������ͼ��ʾ��

�ٴӷ�Ӧ��ʼ��a��ʱ��ƽ����Ӧ����v(CO)=__________��
��b��ʱ��CO ��ת����Ϊ_____________��
��b�� �� d�� �� ��ѧ ƽ�ⳣ��:Kb____(� >����<����=�� )Kd���жϵ�������_____________________��
����Ŀ����2 L�ܱ������У�800 ��ʱ��Ӧ2NO(g)+O2(g)![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

��Ӧ������ͼ��ʾ������ֻ��3����������ȷ�ġ���ش�
(1)A�㴦��v������____v���棩 ��������������С������������������ͬ����A������Ӧ����_______B������Ӧ���ʡ�
(2)ͼ�б�ʾNO2�ı仯��������___����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v=__��
(3)��˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����________ ������ĸ����
a.v��NO2��=2v��O2�� b.������ѹǿ���ֲ���
c.v����NO��=2v����O2�� d.�����ڵ��ܶȱ��ֲ���
(4)��ʹ�÷�Ӧ�ķ�Ӧ�����������________������ĸ����
a.��ʱ�����NO2���� b.�ʵ������¶�
c.��СO2��Ũ�� d.ѡ���Ч�Ĵ���