题目内容
化学家鲍林在研究含氧酸的强弱时,提出了一个定性规则:含氧酸分子中的非羟基(注:羟基是-OH)氧原子数与酸性强弱成相关性.设含氧酸化学式为HnROm,则非羟基氧原子数为(m-n),其数值越大,该含氧酸的酸性越强.鲍林认为含氧酸的强弱与非羟基氧原子数(m-n)有如下关系:
(1)规则判断H3AsO4、H2CrO4、HMnO4酸性由强到弱的顺序为 .
*(2)H3PO3和H3AsO3的形式一样,分子结构相同,但酸性强弱相差很大,已知H3PO3为中强酸,H3AsO3为弱酸.试推断H3PO3和H3AsO3的分子结构式分别为 和 .
| m-n | 0 | 1 | 2 | 3 |
| 含氧酸强度 | 弱 酸 | 中 强 | 强 | 很 强 |
| 实 例 | HClO | H3PO4 | HNO3 | HClO4 |
*(2)H3PO3和H3AsO3的形式一样,分子结构相同,但酸性强弱相差很大,已知H3PO3为中强酸,H3AsO3为弱酸.试推断H3PO3和H3AsO3的分子结构式分别为
考点:化学键
专题:化学键与晶体结构
分析:(1)根据题中非羟基氧原子数与酸性强弱的关系分析;
(2)H3PO3和H3AsO3的酸性不同,说明二者分子中非羟基氧原子数不同,据此分析;
(2)H3PO3和H3AsO3的酸性不同,说明二者分子中非羟基氧原子数不同,据此分析;
解答:
解:(1)由题中表格数据可知,非羟基氧原子数越多,酸性越强,H3AsO4非羟基氧原子数为1,H2CrO4非羟基氧原子数为2,HMnO4非羟基氧原子数为3,则酸性:H3AsO4<H2CrO4<HMnO4,
故答案为:H3AsO4<H2CrO4<HMnO4;
(2)因为酸性H3PO3>H3AsO3,则H3PO3中非羟基氧的数目应大于H3AsO3,且H3AsO3为弱酸,所以可以推知H3AsO3没有非羟基氧,其分子结构分别为: 、
、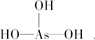 ;
;
故答案为: 、
、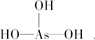 ;
;
故答案为:H3AsO4<H2CrO4<HMnO4;
(2)因为酸性H3PO3>H3AsO3,则H3PO3中非羟基氧的数目应大于H3AsO3,且H3AsO3为弱酸,所以可以推知H3AsO3没有非羟基氧,其分子结构分别为:
 、
、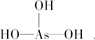 ;
;故答案为:
 、
、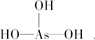 ;
;
点评:本题考查了含有酸酸性的比较,注意对题中信息的提取和应用,明确含氧酸强弱的判断方法即可解答,题目难度中等.

练习册系列答案
相关题目
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、9g D2O中含有的电子数为5NA |
| B、92g NO2和N2O4混合气体中含有原子数为6NA |
| C、1mol C3H8分子中共价键总数为8NA |
| D、65g Zn全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为NA |
常温下,下列溶液中可能大量共存的离子组是( )
| A、水电离产生的c(H+)=1×10-12mol/L的溶液中:AlO2-、S2-、PO43-、Na+ |
| B、加入金属镁能产生H2的溶液中:Na+、HCO3-、SO42-、Al3+ |
| C、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、CO32- |
| D、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
下列物质中不属于合金的是( )
| A、不锈钢 | B、白铜 |
| C、高碳钢 | D、金刚石 |
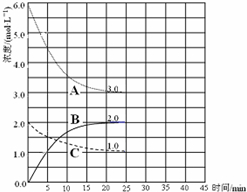 合成氨对农业生产及国防建设均具有重要意义.
合成氨对农业生产及国防建设均具有重要意义.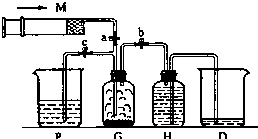 某课外活动小组利用下列装置迅速制备少量氯气.提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体.(2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)试回答:
某课外活动小组利用下列装置迅速制备少量氯气.提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体.(2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)试回答: