题目内容
【题目】A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)B的核外电子有 种空间运动状态;写出F的外围电子排布图: 。
(2)根据等电子体原理,写出B22-离子的电子式: 。
(3)根据价层电子对互斥理论(VSEPR)推测:A2C的VSEPR模型名称: 。
(4)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是 。
(5)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成 δ键和 π键。SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键 。
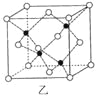
(6)E的一种晶体结构如图甲,则其一个晶胞中含有 个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为 pm。(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)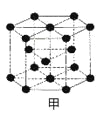
【答案】(1)6![]()
(2)![]()
(3)四面体
(4)HF分子间通过氢键形成缔合分子
(5)C的原子半径较小,C、O原子能充分接近,p-p轨道肩并肩重叠程度较大,形成较稳定的π键,Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不能形成上述稳定的π键
(6)2;
【解析】试题分析: A与其他元素既不同周期又不同族,A是氢;B、C的价电子层中未成对电子数都是2,B是碳,C是氧;E核外的s、p能级的电子总数相等,E是镁 ;F与E同周期且第一电离能比E小,F是铝;G的+1价离子(G+)的各层电子全充满,G是铜。A~G是前四周期除稀有气体之外原子序数依次增大的七种元素,所以D是氟。
(1)碳元素的核外电子排布为1s22s22p2,因此碳原子的核外电子有6种空间运动状态;F是铝原子,所以价电子排布图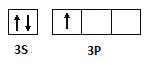 。
。
(2)原子数和价电子数分别均相等的是等电子体,则B22-离子与氮气互为等电子体,则其的电子式为![]() 。
。
(3)水分子中氧原子含有的价层电子对数是4,其中含有2对孤对电子,则其VSEPR模型名称是四面体。
(4)F元素电负性很大,分子之间形成氢键,以形成缔合分子(HF)n,实验测得HF的相对分子质量一般高于理论值;
(5)由于C的原子半径较小,C、O原子能充分接近,p-p轨道肩并肩重叠程度较大,形成较稳定的π键,Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,因此不能形成上述稳定的π键
(6)晶体镁的晶胞是平行六面体,也就是六棱柱的三分之一,所以一个晶胞中含有8×1/8+1=2;CuF晶胞结构知含有4个CuF,设立方体的边长为r,V=![]() =
=![]() =r3,解得立方体的边长为r=
=r3,解得立方体的边长为r=![]() cm,Cu与F的最近的距离是○与●连线,根据数学知识解的Cu与F的最近的距离是
cm,Cu与F的最近的距离是○与●连线,根据数学知识解的Cu与F的最近的距离是
 。
。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案【题目】TiO2和TiCl4都是钛的重要化合物,某化学兴趣小组在实验室对两者的制备及性质进行探究。
Ⅰ.制备TiCl4
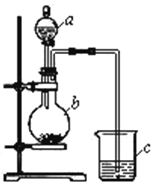
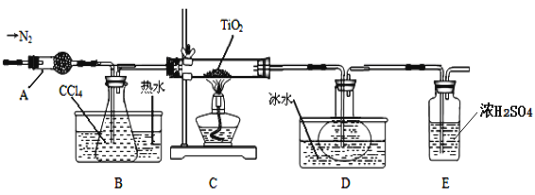
实验室利用反应TiO2 (s)+CCl4(g)![]() TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | —23 | 76 | 与TiCl4互溶 |
TiCl4 | —25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题:
(1)仪器A的名称是 。
(2)实验开始前后的操作包括:①检查装置气密性,②组装仪器,③通N2一段时间,④加装药品,⑤点燃
酒精灯⑥停止通N2⑦停止加热。正确的操作顺序是__________________________。实验结束后欲分离D中的液态混合物,所采用操作的名称是 。
(3)装置E能否 (填“能”或“不能”)换成装置A,理由是 。
(4)TiCl4是制取航天航空工业材料——钛合金的重要原料。某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素。 。
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2。
(5)写出生成TiO2·xH2O的化学方程式 。
(6)检验沉淀是否洗涤干净的方法是___________________________________________。
(7) 一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取上述TiO2试样0.2g,消耗0.1 mol·L-1 NH4Fe(SO4)2标准溶液20mL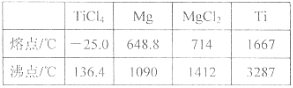 。
。
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是: 。
②该滴定操作所用到的指示剂是 。
③则TiO2质量分数为 。
【题目】下表给出五种短周期元素的相关信息。
元素 | 相关信息 |
A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
D | 室温下其单质为淡黄色粉末状固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
请按要求回答下列问题:
(1)D元素核外电子排布 ;
(2)A、B两元素形成的含有非极性键的化合物的结构式 ;A、B两元素形成的具有相同电子数的离子有(填化学式):______________、_____________。
(3)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1∶2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式: 。
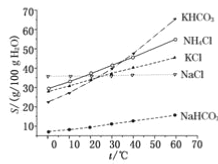
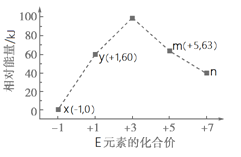
(4)一定条件下,在水溶液中1 mol E-、EO(x=1,2,3,4)的能量(kJ)相对大小如右图所示。n是 (填离子符号)。离子反应y→x+m的热化学方程式为 。
(5)Na2DB3水溶液中各离子浓度的大小顺序是 (填离子符号)