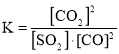题目内容
【题目】第23号元素钒在地壳中的含量大约为0.009%,在过渡元素中仅次于Fe、Ti、Mn、Zn,排第五位。我国四川攀枝花地区蕴藏着极其丰富的钒钛磁铁矿。
(1)钒在周期表中的位置为__________,电子占据的最高能层的轨道形状为__________。
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是__________。
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、__________(任写一个)等。
②CO作配体时,配位原子是C而不是O,其原因是__________。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是__________。
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物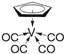 的熔点为138 ℃,其晶体类型为__________;已知该化合物满足18电子规则,其配体“
的熔点为138 ℃,其晶体类型为__________;已知该化合物满足18电子规则,其配体“![]() ”中的大π键可表示为__________。
”中的大π键可表示为__________。
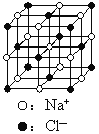
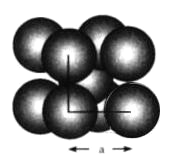
(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。
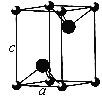
①VCl2和VBr2两者熔点差异的原因是__________。
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为__________(用含a、c、r+和r-的式子表示)。
【答案】 第四周期第VB族 球形 Mn NO+、![]() C的电负性小于O,对孤电子对吸引能力弱,给出电子对更容易 D 分子晶体
C的电负性小于O,对孤电子对吸引能力弱,给出电子对更容易 D 分子晶体 ![]() 两者均为离子晶体,Cl-半径小于Br-半径,VCl2中晶格能大于VBr2,故VCl2熔点高于VBr2
两者均为离子晶体,Cl-半径小于Br-半径,VCl2中晶格能大于VBr2,故VCl2熔点高于VBr2 ![]()
【解析】(1)钒是第23号元素,在周期表中的位置为第四周期第VB族;电子占据的最高能层的轨道是4s轨道,形状为球形;(2)五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数分别为4、2、5、0、3,最多的是Mn;(3)等电子体指价电子数和原子数相同的分子、离子或基团,CO的等电子体有N2、CN-、NO+、![]() ;②CO作配体时,配位原子是C而不是O,其原因是C的电负性小于O,对孤电子对吸引能力弱,给出电子对更容易;(4)①A.[V(H2O)6]2+中V原子为21电子, B.[V(CN)6]4-中V原子为21电子,C.[V(CO)6]-中V原子为24电子D.[V(O2)4]3-中V原子满足18电子规则。答案选D;②化合物
;②CO作配体时,配位原子是C而不是O,其原因是C的电负性小于O,对孤电子对吸引能力弱,给出电子对更容易;(4)①A.[V(H2O)6]2+中V原子为21电子, B.[V(CN)6]4-中V原子为21电子,C.[V(CO)6]-中V原子为24电子D.[V(O2)4]3-中V原子满足18电子规则。答案选D;②化合物 的熔点为138 ℃,低熔点,其晶体类型为分子晶体;已知该化合物满足18电子规则,其配体“
的熔点为138 ℃,低熔点,其晶体类型为分子晶体;已知该化合物满足18电子规则,其配体“![]() ”中的大π键5碳共用5电子,可表示为
”中的大π键5碳共用5电子,可表示为![]() ;(5)①两者均为离子晶体,Cl-半径小于Br-半径,VCl2中晶格能大于VBr2,故VCl2熔点高于VBr2;②晶体中阴、阳离子半径分别为r-和r+,晶胞的体积为
;(5)①两者均为离子晶体,Cl-半径小于Br-半径,VCl2中晶格能大于VBr2,故VCl2熔点高于VBr2;②晶体中阴、阳离子半径分别为r-和r+,晶胞的体积为![]() ,晶胞所占体积为
,晶胞所占体积为![]() ,该晶体的空间利用率为
,该晶体的空间利用率为![]() 。
。

【题目】合成气(CO+H2)广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气。
(1)已知标况下,5.6LCH4与水蒸气完全反应时吸收51.5KJ的热量,请写出该反应的热化学方程式____;
(2)在150℃时2L的密闭容器中,将2 mol CH4和2 mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=____。
②在该温度下,计算该反应的平衡常数K=____。
③下列选项中能表示该反应已达到平衡状态的是____
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C (CH4) = C (CO)
(3)合成气中的氢气也用于合成氨气:N2 + 3H2![]() 2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
容 器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2的 体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | ν甲 | P甲 |
乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | ν乙 | P乙 |
丙 | 2L | 2molN2+6molH2 | n2 mol | span>φ丙 | ν丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.ν乙>ν丙>ν甲 D.P乙>P甲=P丙
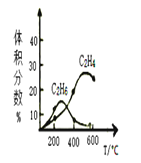
(4)合成气制甲醚的反应方程式为2CO(g) + 4H2(g)![]() CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。
CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。

① 290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是____;
② b____0,(填“>”或“<”或“=”)理由是____。