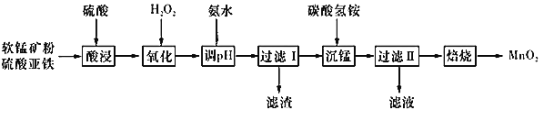
题目内容
【题目】铁和氧化铁的混合物共Xmol,加盐酸后固体全部溶解,共收集到Ymol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则反应后溶液中Fe元素质量为( )
A.56(3X+Y)gB.56(3X-Y)gC.28(3X+Y)gD.28(3X-Y)g
【答案】D
【解析】
根据电子守恒:与H+反应生成H2的铁的物质的量等于氢气的物质的量:n(Fe)=n(H2)=Ymol;
其余的铁则和Fe2O3以等物质的量溶于盐酸生成FeCl2,即Fe+Fe2O3+6H+=3Fe2++3H2O,参加该反应的铁的物质的量为![]() (X-Y)mol,Fe2O3的物质的量也是
(X-Y)mol,Fe2O3的物质的量也是![]() (X-Y)mol,因此共含铁元素Ymol+
(X-Y)mol,因此共含铁元素Ymol+![]() (X-Y)mol+(X-Y)mol=
(X-Y)mol+(X-Y)mol=![]() (3X-Y)mol,所以共含铁元素:
(3X-Y)mol,所以共含铁元素:![]() (3X-Y)mol ×56g/mol=28(3X-Y)g;
(3X-Y)mol ×56g/mol=28(3X-Y)g;
答案选D。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】古埃及人在公元前一千多年前曾用橄榄石(硅酸盐)作饰品,称它为“太阳的宝石”。某小组以某橄榄石(主要成分可看作为MgO、FeO和SiO2,还含有少量的MnO等)为原料制备工业合成氨的活性催化剂(FeO和Fe2O3质量比为9:20的混合物)的一种流程如下:
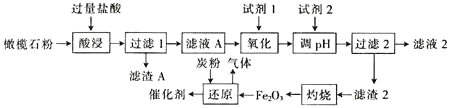
金属离子生成氢氧化物沉淀的pH如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Mg2+ | 7.6 | 9.4 |
Fe2+ | 6.5 | 9.9 |
Fe3+ | 1.5 | 3.3 |
Mn2+ | 8.2 | 10.6 |
回答以下问题:
(1)从绿色化学角度分析,试剂1宜选择___(填字母)。加入试剂1的目的是___(用离子方程式表示)。
a.H2O2 b.MnO2 c.HNO3 d.K2Cr2O7
(2)调节pH范围为___。
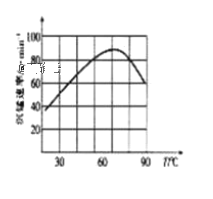
(3)单位时间内“酸浸”中金属浸出率与温度、盐酸浓度的关系如图所示。
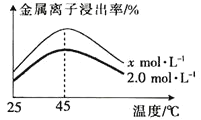
x___(填“>”“<”或“=”)2。当盐酸浓度相同时,温度高于45℃,浸出率降低的主要原因是___。
(4)“还原”过程中,不仅要控制温度,而且要控制氧化铁和炭粉(C)的比例。若“还原”时产生气体的相对分子质量为36,理论上,480kgFe2O3需要加入___kg炭粉(C)。