题目内容
16.欲除去下列物质中的少量杂质,请填写所用方法及化学方程式.| 欲除去的少量杂质 | 方法或试剂 | 反应的化学方程式 |
| (1)Na2CO3固体中的NaHCO3 | ||
| (2)金属Mg中的Al | ||
| (3)NaOH溶液中的Na2CO3 | ||
| (4)CO2中的HCl气体 |
分析 (1)碳酸氢钠不稳定,受热易分解生成Na2CO3;
(2)碳酸钠能和盐酸反应生成氯化钠、水和CO2,所以要除去NaCl溶液中的Na2CO3应用HCl来除去,化学方程式是碳酸钠能和盐酸反应生成氯化钠、水和CO2,所以要除去NaCl溶液中的Na2CO3应用HCl来除去,化学方程式是碳酸钠能和盐酸反应生成氯化钠、水和CO2;
(3)碳酸钠能和石灰水反应生成白色沉淀碳酸钙和氢氧化钠;
(4)NaHCO3溶液能与盐酸反应生成氯化钠、水和二氧化碳.
解答 解:(1)碳酸氢钠不稳定,受热易分解,所以将固体混合物加热,即可将Na2CO3固体中的NaHCO3除去,化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(2)碳酸钠能和盐酸反应生成氯化钠、水和CO2,所以要除去NaCl溶液中的Na2CO3应用HCl来除去,化学方程式是碳酸钠能和盐酸反应生成氯化钠、水和CO2,所以要除去NaCl溶液中的Na2CO3应用HCl来除去,化学方程式是碳酸钠能和盐酸反应生成氯化钠、水和CO2,所以要除去NaCl溶液中的Na2CO3应用HCl来除去,化学方程式是Na2CO3+2HCl═2NaCl+CO2↑+H2O;
(3)碳酸钠能和石灰水反应生成白色沉淀碳酸钙和氢氧化钠,所以将混合液加入适量的石灰水,过滤蒸干即可除去杂质;
(4)NaHCO3溶液能与盐酸反应生成氯化钠、水和二氧化碳,HCl+NaHCO3═NaCl+H2O+CO2↑(H++HCO3-=H2O+CO2↑),在除去氯化氢的同时增加了二氧化碳的量;
故答案为:
| 欲除去的少量杂质 | 方法或试剂 | 反应的化学方程式 |
| (1)Na2CO3固体中的NaHCO3 | 加热 | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O |
| (2)金属Mg中的Al | 加入适量的盐酸至无气体放出 | Na2CO3+2HCl═2NaCl+CO2↑+H2O |
| (3)NaOH溶液中的Na2CO3 | 加入适量的石灰水 | Ca(OH)2+Na2CO3═2NaOH+CaCO3↓ |
| (4)CO2中的HCl气体 | 饱和NaHCO3溶液 | HCl+NaHCO3═NaCl+H2O+CO2↑ |
点评 本题考查物质的分离、提纯和除杂等问题,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案| A. | 明矾水解成Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 通过地沟油(油脂)的碱性水解来制肥皂 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
| A. | 气体单质中一定存在σ键,可能存在π键 | |
| B. | 具有下列价电子排布式的基态原子中,①3s23p1,②3s23p2,③3s23p3,④3s23p4,第一电离能最大的是③ | |
| C. | NH4+和CH4属于等电子体,立体构型都是正四面体 | |
| D. | BF3、NCl3、H2O、XeF4、BeCl2分子中所有原子都满足最外层为8电子结构的是NCl3 |
| A. | ①②③⑤ | B. | ④⑤⑥ | C. | ③⑤ | D. | ②③④⑥ |
| A. | 过氧化氢的电子式为  | B. | 1,3-二甲基丁烷  | ||
| C. | Na+的结构示意图为 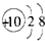 | D. | 乙烯的结构式为 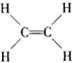 |
| A. | 第七周期ⅠB族 | B. | 第七周期ⅡB族 | C. | 第六周期ⅠB族 | D. | 第六周期ⅡB族 |
| A. | 使用铁触媒 | B. | 提高压强 | C. | 将氨液化分离 | D. | 增大N2浓度 |
| A. | 一定温度下,1L0.5mol•L-1NH4Cl溶液与1L0.25mol•L-1NH4Cl溶液中NH4+物质的量之比为2:1 | |
| B. | 100g硫酸溶液的物质的量浓度为18.4mol/L,用水稀释到物质的量浓度为9.8mol/L,需要水100g. | |
| C. | 标准状况下,22.4LCH3Cl和CHCl3的混合物中所含有的碳原子个数一定为NA | |
| D. | 在2Na2O2+2CO2=2Na2CO3+O2反应中,每生成16g氧气,则转移NA个电子 |