题目内容
15.下列离子方程式书写正确的是( )| A. | 铝与氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ | |
| B. | 向硫酸铝中加入过量氨水:Al3++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| C. | NH4HCO3溶液与足量NaOH溶液共热:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+2H2O+CO32- | |
| D. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+ $\frac{\underline{\;\;△\;\;}}{\;}$ Fe3++3NO2↑+3H2O |
分析 A.电荷、电子不守恒;
B.氢氧化铝与氨水不反应,应生成氢氧化铝;
C.NH4HCO3溶液与足量NaOH溶液共热生成氨气和碳酸钠;
D.加入过量铁粉生成亚铁离子.
解答 解:A.电荷、电子不守恒,反应的离子方程式为2H2O+2Al+2OH-=2AlO2-+3H2↑,故A错误;
B.氢氧化铝与氨水不反应,应生成氢氧化铝,反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C.NH4HCO3溶液与足量NaOH溶液共热生成氨气和碳酸钠,反应的离子方程式为NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+2H2O+CO32-,故C正确;
D.加入过量铁粉,生成亚铁离子,离子反应为Fe+2NO3-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe2++2NO2↑+2H2O,故D错误.
故选C.
点评 本题考查了离子方程式正误判断,明确物质之间的反应、物质的性质及离子方程式的书写即可解答,注意D中铁过量的条件,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=13 的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 甲基橙呈黄色的溶液:Na+、K+、ClO-、AlO2- | |
| C. | 0.1 mol/L 的KNO3 溶液:H+、Fe2+、Cl-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol.L-1的溶液中:K+、Ba2+、Br-、I- |
6.下列实验方法或操作能达到实验目的是( )
| A. | 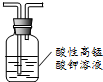 除去甲烷中乙烯 | B. |  制备乙酸乙酯 | ||
| C. |  分离乙酸和水 | D. | 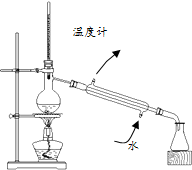 制备蒸馏水 |
10.盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表述正确的是( )
| A. | 10mL0.10mol•L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) | |
| C. | 在NaHCO3溶液中加入等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- | |
| D. | 中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH的物质的量相同 |
20.常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )

| A. | 当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3•H2O)>c(CO32-) | |
| B. | NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3•H2O)+c(H+)=c(OH-)+2c(CO32-)+c(H2CO3) | |
| C. | 往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| D. | 通过分析可知常温下Kb(NH3•H2O)>Ka1(H2CO3) |
7.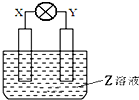 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )| X | Y | Z | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 锌 | 铜 | 硝酸银溶液 |
| D | 碳 | 锌 | 硝酸铜溶液 |
| A. | 锌做负极溶解X电极变轻,错误 | |
| B. | 铁做负极失电子溶解变轻,X电极生成氢气不会变重,错误 | |
| C. | 锌做负极溶解X电极变轻,错误 | |
| D. | 锌做负极失电子发生氧化反应Y棒变轻,碳做正极溶液中铜离子析出使X极变重,正确 |
5.用铁酸钠(Na2FeO4)对自来水消毒是饮用水处理新技术,下列有关分析正确的是( )
| A. | 在Na2FeO4中Fe显+8价,具有强氧化性,所以能杀菌消毒 | |
| B. | 因为Na2FeO4溶液显碱性,所以能杀菌消毒 | |
| C. | Na2FeO4的还原产物为Fe3+,其易水解产生Fe(OH)3胶体,使水中悬浮物聚沉 | |
| D. | Na2FeO4的还原产物Fe2+ 水解,生成的胶体使水中悬浮物沉降,从而达到消毒目的 |
 表示的分子式C6H14结构简式(CH3)2CHCH2CH2CH3名称是2-甲基戊烷.
表示的分子式C6H14结构简式(CH3)2CHCH2CH2CH3名称是2-甲基戊烷.