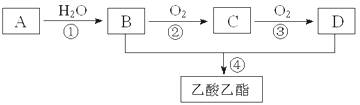
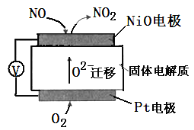
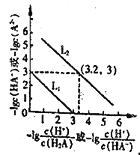
��Ŀ����
����Ŀ����һ�����İ�������粒����������Ƶ��ܱ���������У�����������䣬��������������Բ��ƣ���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4(s)![]() 2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µIJ���ƽ���������±���
2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µIJ���ƽ���������±���
�¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
ƽ����ѹǿ/kPa | 5.7 | p1 | 12.0 | p2 | 24.0 |
ƽ��������Ũ��/10��3 mol��L��1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
����˵���в���ȷ����
A. ��������ƽ����Է�����������M������ʱ��仯ʱ��Ӧ��ƽ��״̬
B. 15.0 ��ʱNH2COONH4(s)�ֽ��ƽ�ⳣ��Ϊ2.0��10��9(mol/L)3
C. �÷�ӦH��0��p2��2p1
D. ���ں����½�ƽ����ϵ������룬�ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���
���𰸡�A
������������A��ֻ�в��������壬�ʷ�Ӧ�����л�������ƽ����Է�����������M����ʱ��仯���ʲ�����ʱ��仯ʱ��Ӧ��ƽ��״̬��A�����B���轫15 ������Ũ��ת��ΪNH3��CO2��Ũ�ȣ�
c��NH3����![]() ��2.4��10��3mol��L��1��1.6��10��3mol��L��1��c��CO2����
��2.4��10��3mol��L��1��1.6��10��3mol��L��1��c��CO2����![]() ��2.4��10��3mol��L��1��0.8��10��3mol��L��1��K����1.6��10��3��2��0.8��10��3��0.2��10��8��B����ȷ��C���¶�����K����Ϊ���ȷ�Ӧ��ƽ����Ũ�Ⱥ�����ǰ�ߵ���������p2��2p1��C����ȷ��D�����ں����½�ƽ����ϵ������룬ƽ��������ƶ������ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���D����ȷ����ѡA��
��2.4��10��3mol��L��1��0.8��10��3mol��L��1��K����1.6��10��3��2��0.8��10��3��0.2��10��8��B����ȷ��C���¶�����K����Ϊ���ȷ�Ӧ��ƽ����Ũ�Ⱥ�����ǰ�ߵ���������p2��2p1��C����ȷ��D�����ں����½�ƽ����ϵ������룬ƽ��������ƶ������ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���D����ȷ����ѡA��

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�����Ŀ������ͼ��ʾװ�ý�������ʵ�飬ʵ������Ԥ�������һ�µ���
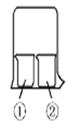
���е����� | ���е����� | Ԥ���������� | |
A | ���۵⻯����Һ | Ũ���� | ���������� |
B | ��̪��Һ | Ũ���� | ���������� |
C | �Ȼ�����Һ | Ũ��ˮ | �а�ɫ���� |
D | ʪ���ֽ�� | ������ˮ | ��ֽ����ɫ |
A. A B. B C. C D. D