题目内容
【题目】已知A是一种气态烃.完全燃烧时产生的水和二氧化碳的物质的量之比为1:1.A的相对分子质量小于30.在下图变化中,中间产物C能和新制的氢氧化铜反应生成砖红色沉淀.(反应条件未写出)
又知2CH3CHO+O2![]() 2CH3COOH.请回答下列问题:
2CH3COOH.请回答下列问题:
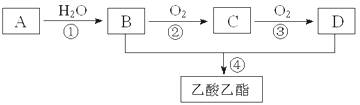
(1)写出A的电子式________
(2)B、D分子内含有的官能团分别是________、________(填名称);
(3)判断下列反应的反应类型:①______________,③______________
(4)写出下列反应的化学方程式:②________________________________________;
(5)下列说法正确的是________。
A.有机物B与金属钠反应,现象是钠浮在液面,不停的游动,最后消失。
B.有机物B、D以及乙酸乙酯可用饱和Na2CO3溶液鉴别
C.反应④中,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
【答案】![]() 羟基 羧基 加成反应 氧化反应 2CH3CH2OH+O2
羟基 羧基 加成反应 氧化反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O BD
2CH3CHO+2H2O BD
【解析】
A是气态烃,完全燃烧时产生的CO2和H2O的物质的量之比为1:1,所以A中C、H原子个数比为1:2,A的相对分子量小于30,所以A是乙烯;中间产物C能和新制氢氧化铜悬浊液产生砖红色沉淀说明C含有醛基,所以C是乙醛,则B是乙醇;乙醇和D反应生成乙酸乙酯,所以D为乙酸,根据题目要求回答问题。
(1)乙烯中含碳碳双键和碳氢单键,电子式为![]() ,
,
故答案为:![]() ;
;
(2)B为乙醇,结构简式为:CH3CH2OH,含官能团为羟基;D为乙酸,结构简式为:CH3COOH,含官能团羧基,
故答案为:羟基;羧基;
(3)乙烯和水生成乙醇的反应是加成反应,乙醛发生催化氧化生成乙酸,为氧化反应,
故答案为:加成反应,氧化反应;
(4)在催化剂、加热条件下,乙醇被氧气氧化生成乙醛,所以反应②的方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(5)A.B为乙醇,钠的密度比乙醇大,乙醇与金属钠反应时,钠沉在下面,故A错误。
B.乙醇和Na2CO3溶液不反应,也不分层,乙酸Na2CO3溶液反应有气泡产生,乙酸乙酯不溶于饱和Na2CO3溶液,所以可用饱和Na2CO3溶液鉴别三种物质,故B正确;
C.在乙酸和乙醇发生的酯化反应中,浓硫酸起催化剂和脱水剂的作用,故C错误;
D.乙醛分子中含有醛基,能被新制碱性氢氧化铜悬浊液、也能被酸性KMnO4溶液氧化,故D正确。
故选BD。

【题目】将一定量的氨基甲酸铵固体置于特制的密闭真空容器中(容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:
2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | p1 | 12.0 | p2 | 24.0 |
平衡气体总浓度/10-3 mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列说法中不正确的是
A. 混合气体的平均相对分子质量——M不再随时间变化时反应达平衡状态
B. 15.0 ℃时NH2COONH4(s)分解的平衡常数为2.0×10-9(mol/L)3
C. 该反应H>0,p2=2p1
D. 若在恒温下将平衡体系体积减半,再达平衡后,c(NH3)和c(CO2)均比原平衡大