题目内容
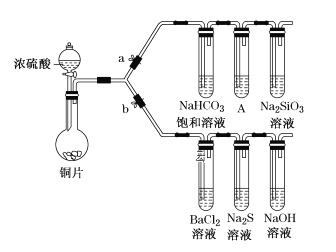
【题目】利用如图所示的实验装置进行实验。
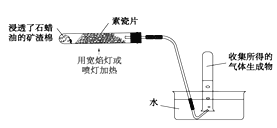
(1)装置中素瓷片的作用____________,矿渣棉的作用__________。
(2)请设计实验证明所得气体生成物中含有不饱和气态烃______。
【答案】作催化剂 作为石蜡油的载体 将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃
【解析】
石蜡油主要含碳、氢元素,经过反应产生能使酸性高锰酸钾溶液褪色的气体,一般是气态不饱和烃,如乙烯或乙炔等。石蜡油分子本身碳原子数较多,经过反应产生乙烯、乙炔等小分子,主要是发生了催化裂化,生成相对分子质量较小、沸点较低的烃。
(1)根据上述分析可知:装置中素瓷片起到了催化剂的作用,矿渣棉用作为石蜡油的载体,故答案:作催化剂;作为石蜡油的载体;
(2)因为石蜡油主要含碳、氢元素,主要是发生了催化裂化,经过反应能生成气态不饱和烃,如乙烯或乙炔等。这些气态不饱和烃能使酸性高锰酸钾溶液褪色,也可以和溴水发生加成反应,所以可以将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃,故答案:将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃。

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目