题目内容
2.材料的不断发展可以促进社会进步,钢铁的生产与使用是人类文明和生活进步的一个重要标志.钢铁在潮湿空气中易发生电化学腐蚀(填“化学”或“电化学”),其负极反应式是Fe-2e-=Fe2+,形成的铁锈的主要成分是Fe2O3.为防止轮船的船体在海水中腐蚀,一般在船身连接锌块(填“锌块”或“铜块”).分析 钢铁在潮湿空气中形成原电池,所以易发生电化学腐蚀,其负极反应式是Fe-2e-=Fe2+,形成的铁锈的主要成分是Fe2O3.为防止轮船的船体在海水中腐蚀,一般使船身作正极被保护,据此分析.
解答 解:钢铁在潮湿空气中形成原电池,所以易发生电化学腐蚀,其负极反应式是Fe-2e-=Fe2+,形成的铁锈的主要成分是Fe2O3.为防止轮船的船体在海水中腐蚀,一般使船身作正极被保护,所以选比铁活泼的锌块,故答案为:电化学;Fe-2e-=Fe2+;Fe2O3; 锌块.
点评 本题考查学生金属的腐蚀和防护以及铝热反应的原理知识,属于基本知识的考查,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.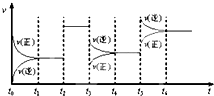 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )| A. | t3 时减小了压强 | |
| B. | t5 时增大了压强 | |
| C. | t6 时刻后反应物的转化率最低 | |
| D. | t1-t2 时该反应的平衡常数大于 t6时反应的平衡常数 |
17.要想除去氯气中含有少量的氯化氢气体最好让气体通过( )
| A. | 氨水 | B. | 浓硫酸 | C. | 饱和氯化钠溶液 | D. | 饱和石灰水 |
7.下列实验操作或分离方法错误的是( )
| A. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时应使温度计水银球靠近蒸馏烧瓶支管口处 | |
| C. | 提取溴水中的溴:加入适量乙醇,振荡、静置、分液 | |
| D. | 用结晶、重结晶除去KNO3中的少量NaCl杂质 |
14.下列反应既是氧化还原反应,又是放热反应的是( )
| A. | 氢氧化钠与稀硫酸反应 | B. | 灼热的炭与水蒸气反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl的反应 | D. | 甲烷在O2中的燃烧 |
11.有人欲配制浓度较大的含有四种不同阴、阳离子的溶液,其中能配制成功的是( )
| A. | K+、H+、Cl-、CO32- | B. | Fe2+、Al3+、Cl-、SO42- | ||
| C. | Na+、Cu2+、NO3-、OH- | D. | NH4+、Ba2+、CO32-、OH- |