题目内容
12.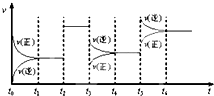 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )| A. | t3 时减小了压强 | |
| B. | t5 时增大了压强 | |
| C. | t6 时刻后反应物的转化率最低 | |
| D. | t1-t2 时该反应的平衡常数大于 t6时反应的平衡常数 |
分析 t2时刻,改变条件时,正逆反应速率都增大且仍然相等,说明平衡不移动,该反应前后气体计量数之和改变,所以改变的条件只能是催化剂;
t3时刻,改变条件时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向元素,该反应的正反应是放热反应,则改变的条件应该是压强;
t5时刻,改变条件时,正逆反应速率都增大,正反应速率大于逆反应速率,平衡正向移动,改变的条件应该是温度.
解答 解:t2时刻,改变条件时,正逆反应速率都增大且仍然相等,说明平衡不移动,该反应前后气体计量数之和改变,所以改变的条件只能是加入催化剂;
t3时刻,改变条件时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向元素,该反应的正反应是放热反应,则改变的条件应该是降低压强;
t5时刻,改变条件时,正逆反应速率都增大,正反应速率大于逆反应速率,平衡正向移动,改变的条件应该是升高温度,
A.通过以上分析知,t3 时减小了压强,故A正确;
B.通过以上分析知,t5 时升高温度,故B错误;
C.t2时刻平衡不移动,t3、t5时刻平衡逆向移动,所以t6时刻后参加反应的反应物物质的量最少,则反应物的转化率最低,故C正确;
D.该反应的正反应是放热反应,升高温度,平衡常数减小,t1-t2时温度小于t6时,所以t1-t2 时该反应的平衡常数大于 t6时反应的平衡常数,故D正确;
故选B.
点评 本题考查图象分析,为高频考点,侧重考查学生分析判断能力,明确外界条件对反应速率影响、平衡移动影响即可解答,难点是平衡移动原理的灵活运用,题目难度不大.

练习册系列答案
相关题目
3.室温下,设1LpH=6的AlCl3溶液中,由水电离出的H+物质的量为n1;1LpH=6的HCl溶液中,由水电离出的H+物质的量为n2.则$\frac{{n}_{1}}{{n}_{2}}$的值是( )
| A. | 1 | B. | 100 | C. | 1000 | D. | 10000 |
20.下列实验,所选装置合理的是
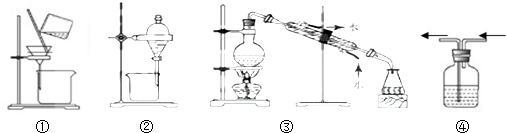 ( )
( )
 ( )
( )| A. | 提纯含NaCl的氢氧化铁胶体用装置① | |
| B. | 分离碘的四氯化碳溶液用② | |
| C. | 分离NaCl的酒精溶液用装置③ | |
| D. | 除去Cl2中的HCl气体用装置④ |
7.下列属于吸热反应的是( )
| A. | 镁条在空气中燃烧 | B. | 盐酸与NaOH溶液反应 | ||
| C. | 酒精在空气中燃烧 | D. | Ba(OH)2?8H2O晶体与NH4Cl晶体反应 |
17.下列反应类型错误的是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ 中和反应 | |
| B. | H2+CuO $\frac{\underline{\;△\;}}{\;}$ Cu+H2O 置换反应 | |
| C. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ 分解反应 | |
| D. | CuO+H2SO4═CuSO4+H2O 复分解反应 |
4.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 标况下,22.4 L水中氢原子原子数大于1NA | |
| B. | 1LpH=1的醋酸溶液中H+数目为0.1NA | |
| C. | 10g46%的甲酸(HCOOH)水溶液中所含氧原子数为0.5 NA | |
| D. | 1molFe溶于稀硝酸过程中电子转移数为2 NA |
1.同温同压下,如果两种气体的体积不相同,其主要原因是( )
| A. | 分子大小不同 | B. | 分子间的平均距离不同 | ||
| C. | 分子性质不同 | D. | 分子数目不同 |
