题目内容
10.下列五组物质,每组中有一种物质从某种角度分析与其它四种不同,请找出该物质填在后面的空白处:(1)Fe、S、C、PFe;
(2)HCl、H2SO4、HNO3、NaHSO4NaHSO4;
(3)空气、氢气、碘酒、盐酸.氢气;
(4)Ag2CO3、BaSO4、NaNO3、CaCO3NaNO3;
(5)CuSO4、Fe(NO3)3、KMnO4、Na2CO3Na2CO3.
分析 (1)依据元素类别分析;
(2)溶液中电离出的阳离子全部是氢离子的化合物为酸,金属阳离子和酸根阴离子构成的化合物为盐;
(3)不同物质组成的为混合物,同种物质组成的为纯净物;
(4)根据盐的溶解性分析;
(5)根据盐的颜色分析,碳酸钠溶液为无色溶液.
解答 解:(1)Fe属于金属元素形成的单质,S、C、P属于非金属元素形成的单质;
故答案为:Fe;
(2)HCl、H2SO4、HNO3属于酸,NaHSO4属于酸式盐,
故答案为:NaHSO4;
(3)空气、氢气、碘酒、盐酸中空气、碘酒、盐酸属于混合物,氢气是纯净物,
故答案为:H2;
(4)Ag2CO3、BaSO4、CaCO3,属于难溶的盐,KNO3是易溶于水的盐;
故答案为:KNO3;
(5)CuSO4、Fe(NO3)3、KMnO4都是有颜色的盐,Na2CO3 属于无色晶体;
故答案为:K2CO3.
点评 本题考查物质的分类,题目难度不大,注意酸、碱、盐以及氧化物,的概念的区别和联纯净物和混合物、单质和化合物的区别联系.

练习册系列答案
相关题目
20.下列实验,所选装置合理的是
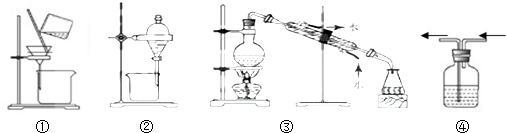 ( )
( )
 ( )
( )| A. | 提纯含NaCl的氢氧化铁胶体用装置① | |
| B. | 分离碘的四氯化碳溶液用② | |
| C. | 分离NaCl的酒精溶液用装置③ | |
| D. | 除去Cl2中的HCl气体用装置④ |
1.同温同压下,如果两种气体的体积不相同,其主要原因是( )
| A. | 分子大小不同 | B. | 分子间的平均距离不同 | ||
| C. | 分子性质不同 | D. | 分子数目不同 |
18.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 常温常压下,28gC2H4和CO的混合气体中含有碳原子的数目为1.5NA | |
| B. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 1mol甲烷分子所含碳氢键数为4NA | |
| D. | 标准状况下,22.4L乙醇的分子数为NA |
5.下列说法正确的是( )
| A. | 固体硝酸钾不导电,所以硝酸钾是非电解质 | |
| B. | 石墨能导电,所以石墨是电解质 | |
| C. | CO2的水溶液能导电,故CO2是电解质 | |
| D. | 盐酸能导电,故氯化氢是电解质 |
19.下列事实中一定能证明HClO是弱电解质的是( )
(1)pH相等的H2SO4和HClO与足量的强碱反应,HClO消耗的强碱体积大
(2)100℃,NaClO溶液的pH=7
(3)NaClO溶液中有HClO分子存在
(4)HClO溶液有很强的氧化性
(5)等体积,等物质的量浓度的HClO与NaOH溶液恰好完全反应
(6)盐酸与KClO溶液反应,生成HClO.
(1)pH相等的H2SO4和HClO与足量的强碱反应,HClO消耗的强碱体积大
(2)100℃,NaClO溶液的pH=7
(3)NaClO溶液中有HClO分子存在
(4)HClO溶液有很强的氧化性
(5)等体积,等物质的量浓度的HClO与NaOH溶液恰好完全反应
(6)盐酸与KClO溶液反应,生成HClO.
| A. | (1)(2)(3) | B. | (1)(3)(4)(6) | C. | (1)(2)(5)(6) | D. | (1)(2)(3)(6) |
20.pH=1.00和pH=3.00的两种强电解质溶液等体积混合溶液的pH为( )
| A. | 2.00 | B. | 1.30 | C. | 4.00 | D. | 5.00 |