题目内容
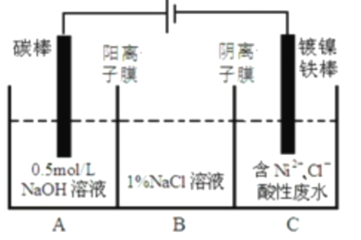
【题目】钛酸钡(BaTiO3)作为著名的铁电和压电材料,因其优异电性能和低污染性受到人们重视,也是目前制备无铅压电陶瓷的重要候选材料。某工厂以重晶石(主要含BaSO4)为原料,生产钛酸钡的工艺流程如图:

回答下列问题:
(1)酸浸时将BaCO3研成粉末并适当增大盐酸浓度,是为了___;常温下,TiCl4为液体且极易水解,配制一定浓度的TiCl4溶液的方法是__。
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=__(填写计算结果);若不考虑CO32-的水解,要使2.33gBaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol·L-1Na2CO3溶液__mL。(已知:Ksp(BaSO4)=1.0×10-10、Ksp(BaCO3)=5.0×10-9)
(3)流程中“滤液"的主要成分为__;隔绝空气煅烧草酸氧钛钡晶体得到钛酸钡粉体和混合气态产物,试写出反应的化学方程式:__。
【答案】提高BaCO3的酸浸速率 溶于浓盐酸,再加适量蒸馏水稀释至所需浓度 0.02 510 NH4Cl BaTiO(C2O4)2·4H2O![]() BaTiO3+2CO↑+2CO2↑+4H2O
BaTiO3+2CO↑+2CO2↑+4H2O
【解析】
(1)根据物质的存在状态及影响化学反应速率的因素分析;TiCl4是强酸弱碱盐,在溶液中弱碱阳离子水解,从抑制盐水解考虑;
(2)根据沉淀的转化平衡方程式书写、计算;
(3)根据原子守恒判断滤液中的主要成分;草酸氧钛钡晶体隔绝空气煅烧得到BaTiO3,同时得到CO、CO2及水蒸气。
(1)盐酸与BaCO3发生反应:2HCl+BaCO3=BaCl2+H2O+CO2↑,为了加快反应速率可以将固体BaCO3研成粉末,以增大接触面积,故答案为:提高BaCO3的酸浸速率;TiCl4是强酸弱碱盐,在溶液中Ti4+会发生水解反应:Ti4++4H2O![]() Ti(OH)4+4H+,使溶液变浑浊,为了配制得到澄清的TiCl4溶液,同时不引入杂质离子,通常是将TiCl4溶于浓盐酸中,然后再加适量水稀释至所需浓度,故答案为:溶于浓盐酸,再加适量蒸馏水稀释至所需浓度;
Ti(OH)4+4H+,使溶液变浑浊,为了配制得到澄清的TiCl4溶液,同时不引入杂质离子,通常是将TiCl4溶于浓盐酸中,然后再加适量水稀释至所需浓度,故答案为:溶于浓盐酸,再加适量蒸馏水稀释至所需浓度;
(2) 在溶液中BaSO4存在沉淀溶解平衡,当向溶液中加入饱和Na2CO3溶液时,发生沉淀转化生成BaCO3:BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq),待达到平衡后,移走上层清液,重复多次操作,最终BaSO4生成BaCO3;反应的平衡常数
BaCO3(s)+SO42-(aq),待达到平衡后,移走上层清液,重复多次操作,最终BaSO4生成BaCO3;反应的平衡常数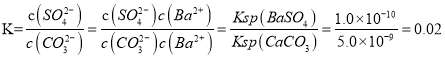 ,故答案为:0.02;2.33gBaSO4物质的量为0.01mol,根据BaSO4(s)+CO32-(aq)
,故答案为:0.02;2.33gBaSO4物质的量为0.01mol,根据BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq),完全转化需要0.01molCO32-,同时溶液中产生0.01molSO42-,根据K值溶液中含有n(CO32-)=0.01mol÷0.02=0.5mol,需要加入Na2CO3为0.01mol+0.5mol=0.51mol,需要Na2CO3溶液的体积为0.51mol÷1mol/L=0.51L=510mL,故答案为:510;
BaCO3(s)+SO42-(aq),完全转化需要0.01molCO32-,同时溶液中产生0.01molSO42-,根据K值溶液中含有n(CO32-)=0.01mol÷0.02=0.5mol,需要加入Na2CO3为0.01mol+0.5mol=0.51mol,需要Na2CO3溶液的体积为0.51mol÷1mol/L=0.51L=510mL,故答案为:510;
(3) TiCl4和草酸混合液加入了氨水,然后与BaCl2溶液混合得到草酸氧钛钡晶体,根据原子守恒,滤液中主要成分为NH4Cl,故答案为:NH4Cl;草酸氧钛钡晶体隔绝空气煅烧得到BaTiO3,同时得到CO、CO2及水蒸气,煅烧草酸氧钛钡晶体得到BaTiO3方程式为BaTiO(C2O4)2·4H2O ![]() BaTiO3+2CO↑+2CO2↑+4H2O,故答案为:BaTiO(C2O4)2·4H2O
BaTiO3+2CO↑+2CO2↑+4H2O,故答案为:BaTiO(C2O4)2·4H2O![]() BaTiO3+2CO↑+2CO2↑+4H2O。
BaTiO3+2CO↑+2CO2↑+4H2O。

【题目】三氯化磷![]() 和三氯氧磷
和三氯氧磷![]() ,是两种重要的化工原料。
,是两种重要的化工原料。
(1)实验室制备![]() 的装置图(如图)和有关信息如下:
的装置图(如图)和有关信息如下:

物质 | 熔点/℃ | 沸点/℃ | 密度 | 性质 |
白磷 | 44.1 | 280.5 | 1.82 | 湿空气中约40℃着火 |
|
| 74.2 | 1.574 | 无色液体,遇水均剧烈水解,互溶 |
| 2.0 | 105.3 | 1.675 |
①实验开始先打开![]() 通入
通入![]() 排除装置内空气的目的是______________________。
排除装置内空气的目的是______________________。
②实验制得的粗产品中含有![]() ,可用_______方法提纯。
,可用_______方法提纯。
③![]()
![]() 和
和![]() ,水解后的溶液中除
,水解后的溶液中除![]() 之外其他离子的浓度由大到小的顺序是___________________________________(已知
之外其他离子的浓度由大到小的顺序是___________________________________(已知![]() 是二元弱酸)。
是二元弱酸)。
(2)实验室通常用![]() 直接氧化
直接氧化![]() 制备
制备![]() ,工业上通常采用潮湿的
,工业上通常采用潮湿的![]() 氧化
氧化![]() 制备
制备![]() ,请写出工业制备的反应方程式:______________________________________。从原理上分析,实验室制备方法的优点是_________________________________________________(写出两点)。
,请写出工业制备的反应方程式:______________________________________。从原理上分析,实验室制备方法的优点是_________________________________________________(写出两点)。
(3)用![]() 标准溶液定量测定实验室制备的
标准溶液定量测定实验室制备的![]() 粗产品的纯度,实验步骤如下:
粗产品的纯度,实验步骤如下:
①取![]() 粗产品溶于水至完全水解,预处理排除磷酸根离子的影响,加入
粗产品溶于水至完全水解,预处理排除磷酸根离子的影响,加入![]() 溶液,完全反应后加少量硝基苯,用力摇动,静置,使沉淀表面被有机物覆盖,防止实验测得的
溶液,完全反应后加少量硝基苯,用力摇动,静置,使沉淀表面被有机物覆盖,防止实验测得的![]() 纯度___________(填“偏大”“偏小”或“不变”)。[已知:
纯度___________(填“偏大”“偏小”或“不变”)。[已知:![]() ]
]
②滴加![]() 作指示剂,用
作指示剂,用![]() 溶液滴定过量的
溶液滴定过量的![]() 溶液,当溶液__________________________,即为终点。共用去
溶液,当溶液__________________________,即为终点。共用去![]() 溶液,则粗产品中
溶液,则粗产品中![]() 的纯度为_________%(保留小数点后1位)。
的纯度为_________%(保留小数点后1位)。