题目内容
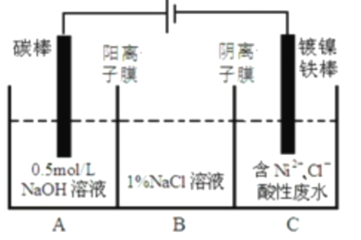
【题目】工业上用电解法处理含镍酸性废水并得到单质![]() 的原理如图所示。下列说法不正确的是( )
的原理如图所示。下列说法不正确的是( )
已知:①![]() 在弱酸性溶液中发生水解;②氧化性:
在弱酸性溶液中发生水解;②氧化性:![]() (高浓度)
(高浓度)![]() (低浓度)。
(低浓度)。
A.电解过程中,B中![]() 溶液的物质的量浓度将不断增大
溶液的物质的量浓度将不断增大
B.碳棒上发生的电极反应:![]()
C.为了提高![]() 的产率,电解过程中需要控制废水的
的产率,电解过程中需要控制废水的![]()
D.该装置中电子的流向:电源负极→阴极→阳极→电源正极
【答案】D
【解析】
A.电解池在工作时,阳离子向阴极移动,阴离子向阳极移动,因此![]() 穿过阳离子膜,流入B室,
穿过阳离子膜,流入B室,![]() 穿过阴离子膜,流入B室,因此氯化钠的浓度增大,A项正确;
穿过阴离子膜,流入B室,因此氯化钠的浓度增大,A项正确;
B.阳极是惰性电极,因此只能是溶液中的![]() 失电子,B项正确;
失电子,B项正确;
C.根据题目给的信息,![]() 会在弱酸性溶液中水解,因此需要控制pH,提高产率,C项正确;
会在弱酸性溶液中水解,因此需要控制pH,提高产率,C项正确;
D.根据“电子不下水,离子不上岸”的原则,电子不可能从阴极流向阳极,D项错误;
答案选D。

【题目】某小组同学探究铁离子与硫离子的反应,实验操作及现象如表:下列有关说法错误的( )
| 滴入FeCl3溶液立刻有黑色沉淀生成继续滴入FeC13溶液,黑色沉淀增多后又逐渐转化为黄色沉淀 |
| 滴入Na2S溶液立刻生成黑色沉淀,沉淀下沉逐渐转化为黄色。继续滴入Na2S溶液,最后出现黑色的沉淀 |
A.两次实验中,开始产生的黑色沉淀都为Fe2S3
B.两次实验中,产生的黄色沉淀是因为发生了反应Fe2S3+4FeCl3═6FeCl2+3S
C.向稀FeCl3溶液中逐滴加入稀Na2S溶液至过量最后生成的黑色沉淀为FeS
D.在Na2S溶液过量的情况下,黑色沉淀中存在较多的Fe(OH)3
【题目】(1)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4 kJ/mol,其化学平衡常数K与温度t的关系如下表:
2NH3(g)△H=-92.4 kJ/mol,其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | ...... |
K/(mol/L)2 | 4.1×106 | K1 | K2 | ...... |
完成下列问题:
①比较K1、K2的大小:K1_______K2(填“>”、“=”或“<”);
②在恒温恒压下判断该反应达到化学平衡状态的依据是_______(填序号);
A 2v(H2)(正)=3v(NH3)(逆)
B 2v(N2)(正)=v(H2)(逆)
C 容器内压强保持不变
D 混合气体的密度保持不变
(2)工业上生产尿素的化学方程式为:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,反应达到平衡时,c(NH3)=0.5mol·L-1,则该反应的平衡常数K=_______。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3molNH3,则此时反应的v正_______v逆(填“>”“<”或“=”)。
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,反应达到平衡时,c(NH3)=0.5mol·L-1,则该反应的平衡常数K=_______。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3molNH3,则此时反应的v正_______v逆(填“>”“<”或“=”)。
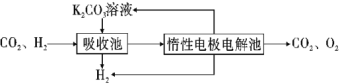
(3)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。
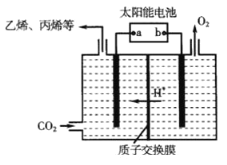
①该工艺中能量转化方式主要有_______。
②电解时,生成乙烯的电极反应式是_______。
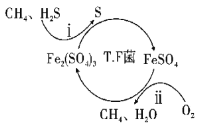
【题目】![]() 、
、![]() 和
和![]() 在工业生产中有重要的应用。
在工业生产中有重要的应用。
(1)用![]() 处理废气中的
处理废气中的![]() 会生成
会生成![]() 、
、![]() 两种单质。在该反应中,氧化剂与还原剂的物质的量之比为_________________________。
两种单质。在该反应中,氧化剂与还原剂的物质的量之比为_________________________。
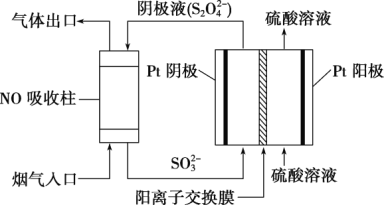
(2)利用![]() 可消除
可消除![]() 污染,其反应为
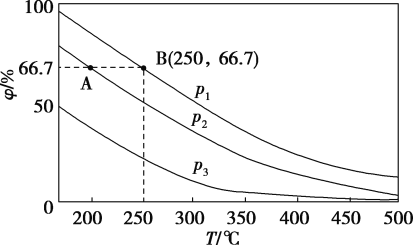
污染,其反应为![]() ,不同温度下,向装有足量
,不同温度下,向装有足量![]() 固体的
固体的![]() 恒容密闭容器中通入
恒容密闭容器中通入![]() ,测得
,测得![]() 气体的体积分数
气体的体积分数![]() 随时间
随时间![]() 的变化曲线如图所示。
的变化曲线如图所示。

①温度为T2时,![]() 内,
内,![]() 的平均反应速率
的平均反应速率![]() _____________________。
_____________________。
②该反应的![]() ________0(填“>”“<”或“=”),判断的理由是_________________。
________0(填“>”“<”或“=”),判断的理由是_________________。
(3)常温下,已知![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() ,通过计算可得
,通过计算可得![]() 的
的![]() 溶液
溶液![]() ___________。
___________。
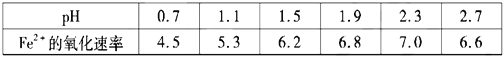
(4)为了确定![]() 氧化速率方程式
氧化速率方程式![]() 中
中![]() 的值(取整数),进行了相应实验。当溶解
的值(取整数),进行了相应实验。当溶解![]() 的浓度为
的浓度为![]() 时,
时,![]() 与速率(
与速率(![]() )数值的关系如下表所示,则
)数值的关系如下表所示,则![]() _______。
_______。
| 3.65 | 7.30 | 10.95 | 14.60 |
| 10.2 | 40.80 | 91.80 | 163.20 |
(5)某工业废水中含有![]() 、
、![]() 等离子。取一定量的该工业废水,向其中滴加
等离子。取一定量的该工业废水,向其中滴加![]() 溶液,当
溶液,当![]() 开始沉淀时,溶液中
开始沉淀时,溶液中 _______(保留两位有效数字)。(已知:25℃时,
_______(保留两位有效数字)。(已知:25℃时, ,
,![]() )
)