题目内容
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”,现邀你一起走进他的化学课堂。
(1)课前老师布置了下列预习作业,请你一起完成:
①铁不同价态的物质各写一种(并标出铁元素的化合价):_____、_______、 ________。
②写出一个它们之间相互转化(含三种价态)的化学方程式:___________________ 。
(2)实验室提供的下列试剂:锌粒、铁粉、0.1 mol·L-1 FeCl3溶液、0.1 mol·L-1 FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性。
根据氧化还原反应的有关原理,小明说Fe2+既有还原性又有氧化性,为证实自己的假设,请你和小明一起设计实验方案,进行实验并描述实验现象,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe2+具有还原性 | 取少量0.1 mol·L-1 FeCl2溶液,加入足量__________后,再往溶液中加入少量__________ | 溶液变成血红色 |
| 探究Fe2+具有氧化性 | 取少量0.1 mol·L-1 FeCl2溶 液,加入_________充分 反应 | 溶液由浅绿色变无色 所发生反应离子方程式为________________ [来源:Z|xx|k.Com] |
(1)①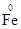
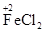
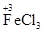 (其他合理的答案也可)②Fe+2FeCl3=3FeCl2
(其他合理的答案也可)②Fe+2FeCl3=3FeCl2
(2)实验方案 实验现象 取少量0.1 mol·L-1 FeCl2溶液,加入足量新制氯水后,再往溶液中加入少量KSCN溶液 加入氯水后,溶液由浅绿色变黄色,再加入少量KSCN溶液后溶液变红色 取少量0.1 mol·L-1 FeCl2溶液,加入锌粒充分反应 加入锌粒后,溶液由浅绿色变无色Fe2++Zn=Fe+Zn2+
解析试题分析:(1)铁常见的化合价就只有三种:零价、正二价、正三价;金属铁还原三价铁离子成二价铁离子就是一个三种化合价的铁都有的铁的反应方程式;
(2)还原性的检验是用氯水来氧化二价铁离子,氧化性的检验是用多属单质来还原三价铁离子。
考点:考查二价铁和三价铁的检验。

 阅读快车系列答案
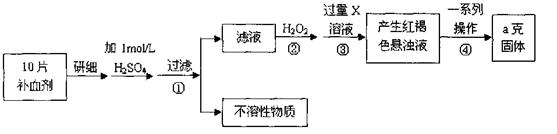
阅读快车系列答案铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。实验室现有下列试剂:0.01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分。
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有_________中的一种或两种。
| | 实验操作 | 预期现象 | 结论 |
| 验证猜想Ⅰ | 步骤①:取少量0.01 mol/L酸性KMnO4溶液,滴入所得溶液 | | |
| 步骤②:_________ | | 含有Fe3+ | |
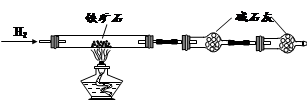
| 验证猜想Ⅱ | 将所得气体通入如下装置 | | 含有两种气体 |
【实验探究】

【问题讨论】
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,判断该方法是否正确并进行评价:_________。
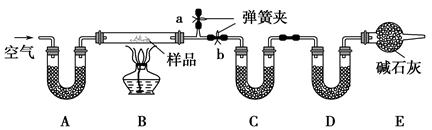
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下: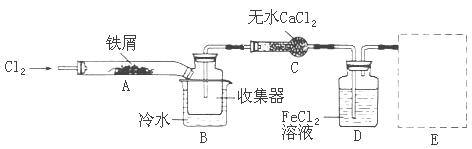
①检查装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成
④ ……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封
请回答下列问题:
(1)写出FeCl3溶液吸收有毒的H2S的离子方程式为
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A的右端。要使沉积得FeCl3进入收集器,第④步操作是
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)
(4)装置B中的冷水作用为 ;装置C的名称为 ;装置D中FeCl2全部反应完后,因为失去吸收Cl2的作用而失效,从下面选出检验FeCl2是否完全失效的试剂:___
| A.氢氧化钠溶液 | B.酸性高锰酸钾溶液 | C.硫氰化钾溶液 | D.氨水 |