题目内容
【题目】海洋资源丰富,海水水资源的利用和海水化学资源(主要为NaCl和MgSO4及K、Br等元素)的利用具有非常广阔的前景。

回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Mg2+和Ca2+,要加入的试剂分别为__________________、__________________。
(2)写出步骤Ⅰ中反应的总化学方程式为___________________________________。
(3)简述步骤Ⅱ中能析出KClO3晶体而无其他晶体析出的原因是_____________________________。
(4)已知MgCl2溶液受热时易水解生成Mg(OH)Cl,写出该过程的化学方程式__________________。
(5)为得到无水MgCl2,步骤Ⅲ的操作应为_____________________________。
(6)步骤Ⅳ中,电解熔融MgCl2得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_____。
A.N2 B.H2 C. CO2 D.空气
(7)海水中溴含量为65mg·L-1。若1L海水中95%溴元素被氧化为Br2经热空气吹出,溴单质残留量3%。最后用SO2将90%Br2还原成Br-,所得溶液体积为50mL。此过程的目的为________________。所得溶液中溴离子浓度为海水中溴离子浓度的_____________倍(精确到0.1)。
【答案】 NaOH 溶液 Na2CO3溶液 Cl-+3H2O![]() ClO3-+3H2↑ 此温度下 KClO3溶解度最小 MgCl2+H2O
ClO3-+3H2↑ 此温度下 KClO3溶解度最小 MgCl2+H2O![]() Mg(OH)Cl+HCl↑ 通入氯化氢,蒸发浓缩冷却结晶 B 提高溴水的浓度 16.6倍
Mg(OH)Cl+HCl↑ 通入氯化氢,蒸发浓缩冷却结晶 B 提高溴水的浓度 16.6倍
【解析】试题分析:(1)除去Mg2+和Ca2+,可以用生成氢氧化镁、碳酸钙沉淀的方法;(2)根据电子守恒,步骤Ⅰ中电解氯化钠溶液,生成氯酸钠、氢气;(3)室温下 KClO3溶解度最小;(4)MgCl2溶液受热时易水解生成Mg(OH)Cl和HCl气体;(5)通入氯化氢可以抑制氯化镁水解;(6)根据金属镁的性质分析;(7)1L海水中95%溴元素转移到50mL溶液中,目的提高溴水的浓度;根据溴元素守恒计算溴离子浓度;
解析:(1)NaCl 溶液由粗盐水精制而成,为除去Mg2+和Ca2+,可以加入氢氧化钠溶液、碳酸钠溶液;(2)根据电子守恒,步骤Ⅰ中电解氯化钠溶液,生成氯酸钠、氢气;反应的总化学方程式为Cl-+3H2O![]() ClO3-+3H2↑;(3)室温下 KClO3溶解度最小,所以向氯酸钠溶液中加入氯化钾能析出KClO3晶体而无其他晶体析出;(4)MgCl2溶液受热时易水解生成Mg(OH)Cl和HCl气体,反应的化学方程式是MgCl2+H2O
ClO3-+3H2↑;(3)室温下 KClO3溶解度最小,所以向氯酸钠溶液中加入氯化钾能析出KClO3晶体而无其他晶体析出;(4)MgCl2溶液受热时易水解生成Mg(OH)Cl和HCl气体,反应的化学方程式是MgCl2+H2O![]() Mg(OH)Cl+HCl↑;(5)通入氯化氢可以抑制氯化镁水解,为得到无水MgCl2,步骤Ⅲ的操作应为通入氯化氢,蒸发浓缩冷却结晶;(6)A.Mg与N2反应生成Mg3N2,故A错误; B.H2与Mg不反应,故B正确; C. CO2与Mg反应生成氧化镁和碳,故C错误; D.镁在空气中能燃烧,故D错误。(7)1L海水中95%溴元素转移到50mL溶液中,目的提高溴水的浓度;设所得溶液中溴离子浓度为x mg·L-1,根据溴元素守恒,
Mg(OH)Cl+HCl↑;(5)通入氯化氢可以抑制氯化镁水解,为得到无水MgCl2,步骤Ⅲ的操作应为通入氯化氢,蒸发浓缩冷却结晶;(6)A.Mg与N2反应生成Mg3N2,故A错误; B.H2与Mg不反应,故B正确; C. CO2与Mg反应生成氧化镁和碳,故C错误; D.镁在空气中能燃烧,故D错误。(7)1L海水中95%溴元素转移到50mL溶液中,目的提高溴水的浓度;设所得溶液中溴离子浓度为x mg·L-1,根据溴元素守恒, ![]() ,x=1078.2,所得溶液中溴离子浓度为海水中溴离子浓度的
,x=1078.2,所得溶液中溴离子浓度为海水中溴离子浓度的![]() 16.6倍;
16.6倍;
【题型】综合题
10
【题目】碳和氯元素及其化合物与人类的生产、生活密切相关。
I、氯的化合物合成、转化一直是科学研究的热点。
(1)一定条件下,氯气与氨气反应可以制备氯胺(NH2Cl)气体,己知部分化学键的键能:
化学键 | N—H | CI—Cl | N—Cl | H—Cl |
键能/ kJmol-1 | 391.3 | 243.0 | 191.0 | 431.8 |
则上述反应的热化学方程式为:__________________。
(2)氯胺(g)是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为______________________。
II.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(1)在三个容积均为1L的密闭容器中以不同的氢碳比![]() 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
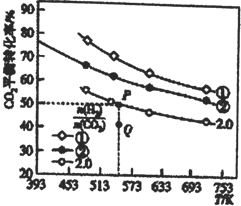
请回答下列问题:
①氢碳比①________②,Q点V(正)___v(逆),该反应的ΔH ________0,(填“大于”或“小于”)
②若起始时,CO2、H2的浓度分别为0.5mol·L-1、l mol·L-1,则P点对应温度的平衡常数的值为_____。P点对应的平衡常数__________Q点对应的平衡常数(填“>”、“<”或“=”)
(2)已知:碳酸H2CO3,K1=4.3×10-7、K2=5.6×10-11
草酸H2C2O4,K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是___________(填字母)。
a.H2CO3、C2O42- b.CO32-、HC2O4- c. C2O42-、HCO3- d.H2C2O4、HCO3-
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是_________________________________。
【答案】 NH3+Cl2=NH2Cl+HCl ΔH=+11.5kJ/mol ![]() > > 小于 29 = a c c(H+)>c(HC2O4-)>c(C2O4-)>c(HCO3-)>c(CO32-)
> > 小于 29 = a c c(H+)>c(HC2O4-)>c(C2O4-)>c(HCO3-)>c(CO32-)
【解析】试题分析:I、(1)根据反应物的总键能—生成物的总键能=焓变,书写热化学方程式;(2)氯胺水解生成氨水和强氧化性的次氯酸;II.(1)①氢气的含量越大,CO2的平衡转化率越大;Q点要达到平衡,CO2的转化率增大,反应正向进行;随温度升高,CO2的平衡转化率减小,平衡逆向移动;②利用“三段式”计算平衡常数;P点、Q点温度相同,对应的平衡常数相同;(2)①根据强酸制取弱酸的规律分析;②根据电离平衡常数分析,
解析:I、(1)NH3+Cl2=NH2Cl+HCl的焓变=![]() kJ/mol,所以热化学方程式是NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g) ΔH=+11.5kJ/mol;(2)氯胺水解生成氨水和强氧化性的次氯酸,水解方程式是
kJ/mol,所以热化学方程式是NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g) ΔH=+11.5kJ/mol;(2)氯胺水解生成氨水和强氧化性的次氯酸,水解方程式是![]() ;II. (1)①氢气的含量越大,CO2的平衡转化率越大,所以氢碳比①>②;Q点要达到平衡,CO2的转化率增大,反应正向进行,V(正)>v(逆);随温度升高,CO2的平衡转化率减小,平衡逆向移动,ΔH <0;
;II. (1)①氢气的含量越大,CO2的平衡转化率越大,所以氢碳比①>②;Q点要达到平衡,CO2的转化率增大,反应正向进行,V(正)>v(逆);随温度升高,CO2的平衡转化率减小,平衡逆向移动,ΔH <0;
②

![]() ;P点、Q点温度相同,平衡常数相同;所以P点对应的平衡常数=Q点对应的平衡常数;(2)①a.草酸的K2大于碳酸的K1,所以H2CO3、C2O42-可以共存;b. 草酸的K2大于碳酸的K2,所以CO32-、HC2O4-不能共存;c. 草酸的K2大于碳酸的K2,所以 C2O42-、HCO3-能共存;d. 草酸的K1大于碳酸的K1,所以H2C2O4、HCO3-不能共存;②草酸的K1>K2大于碳酸的K1>K2,所以等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度由大到小的顺序是c(H+)>c(HC2O4-)>c(C2O4-)>c(HCO3-)>c(CO32-)。
;P点、Q点温度相同,平衡常数相同;所以P点对应的平衡常数=Q点对应的平衡常数;(2)①a.草酸的K2大于碳酸的K1,所以H2CO3、C2O42-可以共存;b. 草酸的K2大于碳酸的K2,所以CO32-、HC2O4-不能共存;c. 草酸的K2大于碳酸的K2,所以 C2O42-、HCO3-能共存;d. 草酸的K1大于碳酸的K1,所以H2C2O4、HCO3-不能共存;②草酸的K1>K2大于碳酸的K1>K2,所以等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度由大到小的顺序是c(H+)>c(HC2O4-)>c(C2O4-)>c(HCO3-)>c(CO32-)。

 阅读快车系列答案
阅读快车系列答案【题目】工业以黄铜矿(主要成分是CuFeS2)为原料制备粗铜,进一步以粗铜为原料制备CuSO4·5H2O晶体。工艺流程如下(部分操作和条件略):
I. 煅烧黄铜矿,得到粗铜(含铁及铁、铜的化合物等);
II. 向粗铜中加入稀H2SO4和稀HNO3,并使产生的NO与H2O、O2反应;
III. 调节Ⅱ中所得溶液的pH,过滤;
Ⅳ. 将Ⅲ中滤液浓缩后冷却结晶,过滤,得到CuSO4·5H2O晶体。
已知:生成氢氧化物的pH
Cu(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.8 | 1.5 |
完全沉淀时 | 6.7 | 2.8 |
注:金属离子的起始浓度为0.1 mol/L
请回答:
(1)I中主要发生如下两个化学反应。请将反应ii的化学方程式补充完整。
i. 2CuFeS2+4O2![]() Cu2S+3SO2+2FeO
Cu2S+3SO2+2FeO
ii. ![]() Cu2S+
Cu2S+![]() O2
O2 ![]()
![]() _________+
_________+ ![]() SO2
SO2
(2)II中NO与H2O、O2反应的化学方程式是_________。
(3)III中的滤渣主要是Fe(OH)3。调节溶液的pH时,pH范围是_________。
(4)有关上述过程的说法中,正确的是_________(填序号)。
a. I中尾气含有SO2,可综合利用制备H2SO4。
b. II中稀HNO3的作用之一是使Cu单质转化为Cu2+
c. 在上述过程中,HNO3可循环利用




