题目内容
14. 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )| A. | 1molN2(g)和1molO2(g)反应放出的能量为180 kJ | |
| B. | 1molN2(g)和1molO2(g)具有的总能量小于2 molNO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和 O2混合能直接生成NO | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
分析 A、分析能量变化黑球代表氧原子,依据反应焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量计算判断;
B、依据A计算的焓变判断反应能量变化,结合反应前后能量守恒分析;
C、氮气和氧气在放电条件才能反应;
D、一氧化氮不能和氢氧化钠反应.
解答 解:A、焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量,N2+O2=2NO,△H=946KJ/mol+498KJ/mol-2×632KJ/mol=180KJ/mol,反应是吸热反应,故A错误;
B、依据A计算可知反应是吸热反应,依据能量守恒,1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量,故B正确;
C、通常情况下,N2(g)和O2(g)混合不能直接生成NO,故C错误;
D、一氧化氮不能和氢氧化钠反应,不是酸性氧化物,故D错误;
故选B.
点评 本题考查了反应能量变化的计算和判断,反应的焓变计算方法和能量守恒是解题关键,题目难度中等.

练习册系列答案
相关题目
4.工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol
(1)要提高CO的转化率,可以采取的措施是df.
a.升温 b.加入催化剂 c.增加CO的浓度
d.充入H2 e.充入惰性气体 f.分离出甲醇
(2)在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温恒容,测得反应达到平衡时的有关数据如表:
下列说法正确的是D.
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
(1)要提高CO的转化率,可以采取的措施是df.
a.升温 b.加入催化剂 c.增加CO的浓度
d.充入H2 e.充入惰性气体 f.分离出甲醇
(2)在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡 时数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的热量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
5.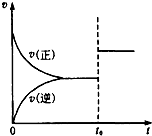 可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )
可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )
 可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )
可逆反应aX(g)+bY(g)?cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如图所示.下列说法中正确的是( )| A. | 若a+b=c,则t0时只增大了反应物的浓度 | |
| B. | 若a+b=c,则t0时只升高了温度 | |
| C. | 若a+b≠c,则t0时只增大了容器的压强 | |
| D. | 若a+b≠c,则t0时只加入了催化剂 |
9.最近,环境保护部向媒体公布了2015年“环境日”“践行绿色生活”主题,该主题旨在增强全民环境意识、节约意识、生态意识,选择低碳、节俭的绿色生活方式和消费模式,形成人人、事事、时时崇尚生态文明的社会新风尚,为生态文明建设奠定坚实的社会和群众基础.下列不符合这一主题的是( )
| A. | 推广节能灯和LED灯泡替代一般白炽灯 | |
| B. | 大力发展地铁,轻轨电车等城市公共交通 | |
| C. | 鼓励购买大排量家庭用燃油汽车 | |
| D. | 提倡使用手帕,减少纸巾的使用 |
19.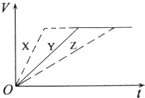 将足量锌块加入到某稀硫酸中,生成氢气的体积(V)与时间(t)的关系如图中曲线Y所示.下列说法正确的是( )
将足量锌块加入到某稀硫酸中,生成氢气的体积(V)与时间(t)的关系如图中曲线Y所示.下列说法正确的是( )
 将足量锌块加入到某稀硫酸中,生成氢气的体积(V)与时间(t)的关系如图中曲线Y所示.下列说法正确的是( )
将足量锌块加入到某稀硫酸中,生成氢气的体积(V)与时间(t)的关系如图中曲线Y所示.下列说法正确的是( )| A. | 反应前,若向稀硫酸中加入少量CuSO4,因CuSO4作催化剂,则关系曲线为X | |
| B. | 反应前,若向稀硫酸中加入少量CuSO4,因增大了c(SO42-),则关系曲线为X | |
| C. | 反应前,若向稀硫酸中加入少量醋酸钠,因生成的醋酸是弱酸,则关系曲线为Z | |
| D. | 反应前,若将纯锌改为粗锌,因粗锌含杂质,则关系曲线为Z |
3.下列反应可以设计成原电池的是( )
| A. | CH4+2O2═CO2+2H2O | B. | NaOH+HCl═NaCl+H2O | ||
| C. | Zn+CuSO4═Cu+ZnSO4 | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
4.下列为某同学利用所学的相关数据进行的推测,其中不正确的是( )
| A. | 根据电解质的电离程度数据推测电解质溶液的导电性 | |
| B. | 用分子所具有能量数据分析分子的稳定性 | |
| C. | 应用固体溶解度数据判断某些复分解反应能否进行 | |
| D. | 利用电解质的电离常数判断某些酸式盐的水溶液的酸碱性 |
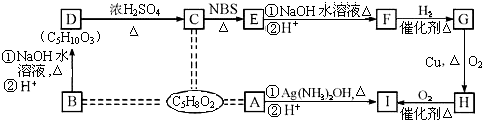
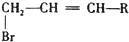
 、HOOCCH2CH2CH2CHO.
、HOOCCH2CH2CH2CHO.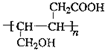 .
.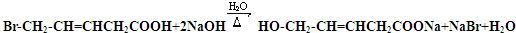 .
.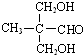 .
.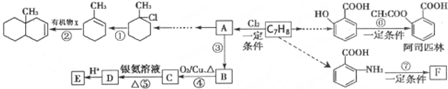

 (苯胺,易被氧化)
(苯胺,易被氧化)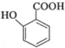 可选用的试剂有(填标号).a.FeCl3溶液 b.浓溴水 c.Na D.NaHCO3溶液
可选用的试剂有(填标号).a.FeCl3溶液 b.浓溴水 c.Na D.NaHCO3溶液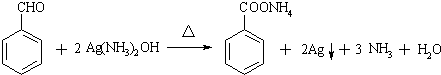 ;
; $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$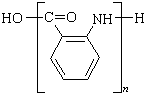 +(n-1)H2O.
+(n-1)H2O. 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用) $→_{△}^{浓硫酸、浓硝酸}$
$→_{△}^{浓硫酸、浓硝酸}$ $\stackrel{酸性高锰酸钾溶液}{→}$
$\stackrel{酸性高锰酸钾溶液}{→}$ $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$