题目内容
15.现有A、B、C、D、E、F六种有机物,它们的转化关系如图所示(图中部分反应条件及生成物没有全部写出).已知:液体B能发生银镜反应,气体D的相对分子质量为28.请回答下列问题:
(1)A、B、C的结构简式分别是CH3CH2OH、CH3CHO、CH3CH2Br.
(2)C→A的反应物及反应条件是NaOH的水溶液,加热.
(3)D→F反应的化学方程式是nCH2=CH2$\stackrel{催化剂}{→}$
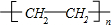 .
.(4)在一定的条件下,A与E反应可生成一种具有香味的物质.该反应的化学方程式是CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
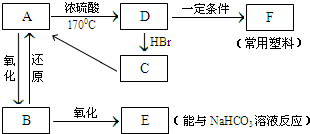
分析 A在浓硫酸、170℃条件下反应生成D,D的相对分子质量是28,则D的结构简式为CH2=CH2,所以A是乙醇,其结构简式为:CH3CH2OH,A发生氧化反应生成B,B能发生银镜反应,则B的结构简式为CH3CHO,B被氧化生成E,E能与碳酸氢钠溶液反应,说明E中含有羧基,则E的结构简式为CH3COOH,乙烯和HBr发生加成反应生成C,C的结构简式为CH3CH2Br,乙烯发生加聚反应生成聚乙烯F,为常用塑料,其结构简式为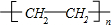 ,结合物质的结构和性质解答.
,结合物质的结构和性质解答.
解答 解:A在浓硫酸、170℃条件下反应生成D,D的相对分子质量是28,则D的结构简式为CH2=CH2,所以A是乙醇,其结构简式为:CH3CH2OH,A发生氧化反应生成B,B能发生银镜反应,则B的结构简式为CH3CHO,B被氧化生成E,E能与碳酸氢钠溶液反应,说明E中含有羧基,则E的结构简式为CH3COOH,乙烯和HBr发生加成反应生成C,C的结构简式为CH3CH2Br,乙烯发生加聚反应生成聚乙烯F,为常用塑料,其结构简式为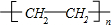 ,
,
(1)通过以上分析知,A的结构简式为CH3CH2OH,B的结构简式为CH3CHO,C的结构简式为CH3CH2Br,故答案为:CH3CH2OH;CH3CHO;CH3CH2Br;
(2)在加热条件下,CH3CH2Br和氢氧化钠的水溶液发生取代反应生成CH3CH2OH,
故答案为:NaOH的水溶液,加热;
(3)在催化剂条件下,乙烯发生加聚反应生成聚乙烯,反应方程式为nCH2=CH2$\stackrel{催化剂}{→}$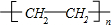 ,
,
故答案为:nCH2=CH2$\stackrel{催化剂}{→}$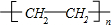 ;
;
(4)乙醇和乙酸反应生成有香味的乙酸乙酯,方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
点评 本题考查了有机物的推断,涉及醇、烯烃、卤代烃、醛、羧酸及高聚物之间的转化,根据A生成D的反应条件结合D的相对分子质量确定A、D的结构简式,再根据各物质之间的转化关系及反应条件确定生成物,明确醇、烯烃、卤代烃、醛、羧酸及高聚物之间知识网络结构是解本题关键,注意:卤代烃在氢氧化钠的水溶液或醇溶液中发生的反应类型不同,其产物不同,为易错点.

 全能练考卷系列答案
全能练考卷系列答案(1)CuS (2)FeS (3)SO3 (4)H2S (5)FeCl2 (6)H2Te.
| A. | (1)(3)(5)(6) | B. | (1)(2)(3)(5) | C. | (1)(2)(4)(5) | D. | 全部 |
| A. | 在水中的溶解度 | B. | 溶液的导电能力 | ||
| C. | 在水中的电离程度 | D. | 化学键的类型 |
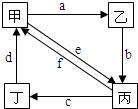 如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| 甲 | 乙 | 丙 | 丁 | |
| ① | Cu | CuO | CuCl2 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 |
| ④ | Al(OH)3 | Al2O3 | NaAlO2 | AlCl3 |
| A. | ①②③④ | B. | 仅②③④ | C. | 仅②④ | D. | 仅③④ |
| A. | 碳酸钠 | B. | 氢氧化钠 | C. | 碳酸氢钠 | D. | 氯化钠 |
| A. | s电子的原子轨道都是球形的,2s电子比1s电子能量高且电子云比1s更扩散 | |
| B. | p电子的原子轨道都是纺锤形的,每个p能级有3个原子轨道,它们相互垂直能量相同 | |
| C. | 当电子排布在同一能级的不同轨道,总是优先单独占据一个轨道,而且自旋方向相反 | |
| D. | 在一个原子轨道里,最多只能容纳2个电子,而且它们的自旋方向相反 |
| A. | 从C(s,石墨)═C(s,金刚石)△H=+1.9 kJ•mol-1,可知石墨比金刚石更稳定 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 | |
| C. | 由H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,可知含1 mol CH3COOH的溶液与含1 mol NaOH的溶液充分混合反应,放出的热量等于57.3 kJ | |
| D. | 2g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ•mol-1 |