题目内容
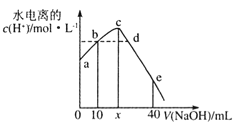
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa,常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA﹣)、pC(A2﹣)变化如图所示,下列说法正确的是

A.随着pH的增大,pC增大的曲线是A2﹣的物质的量浓度的负对数
B.pH=3.50时,c(HA﹣)> c(H2A) > c(A2﹣)
C.b点时c(H2A)·c(A2﹣)/c2(HA﹣)=10﹣4.5
D.pH=3.00~5.30时,c(H2A)+c(HA﹣)+c(A2﹣)先减小后增大
【答案】C
【解析】
H2A存在电离平衡:H2AH++HA-、HA-H++A2-,pH增加促进电离平衡正向移动,所以由图可知:下方曲线是HA-的物质的量浓度的负对数,左侧曲线是H2A的物质的量浓度的负对数,右侧曲线是A2-的物质的量浓度的负对数,由此分析解答。
A.由分析可知,随着pH的增大,pC增大的曲线是H2A的物质的量浓度的负对数,故A错误;
B.pH=3.50时,左侧曲线是H2A的物质的量浓度的负对数,右侧曲线是A2-的物质的量浓度的负对数,此时pC(H2A)>pC(A2-)>pC(HA-),即c(HA-)>c(A2-)>c(H2A),故B错误;
C.b点时,c(H2A)=c(A2-),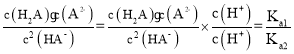 ,交点a处c(HA-)=c(H2A),故Ka1=
,交点a处c(HA-)=c(H2A),故Ka1=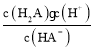 =c(H+)=l×10-0.8,HA-A2-+H+,交点c处c(HA-)=c(A2-),故Ka2=
=c(H+)=l×10-0.8,HA-A2-+H+,交点c处c(HA-)=c(A2-),故Ka2=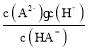 =c(H+)=l×10-5.3,故c(H2A)·c(A2﹣)/c2(HA﹣)=10-0.8/10-5.3=10﹣4.5,故C正确;
=c(H+)=l×10-5.3,故c(H2A)·c(A2﹣)/c2(HA﹣)=10-0.8/10-5.3=10﹣4.5,故C正确;
D.D.pH=3.00~5.30时,结合物料守恒c(H2A)+c(HA-)+C(A2-)始终不变,故D错误;
故答案为C。

练习册系列答案
相关题目