题目内容
【题目】如图是模拟电化学反应装置图。下列说法正确的是( )
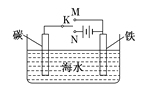
A. 开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+
B. 开关K置于N处,可以减缓铁的腐蚀
C. 开关K置于M处,则铁电极的电极反应式为: 2Cl--2e-=Cl2↑
D. 开关K置于M处,电子从碳棒经开关K流向铁棒
【答案】B
【解析】试题分析:A、开关K置于N处,构成电解池,铁电极为阴极,电极反应为2H2O+2e-=H2↑+2OH-,A错误;B、开关K置于N处,构成电解池,铁电极为阴极,铁的腐蚀减缓,B正确;C、开关K置于M处,构成原电池,铁电极为负极,电极反应式为:Fe-2e-=Fe2+,C错误;D、开关K置于M处,构成原电池,铁电极为负极,电子从铁棒经开关K流向碳棒,D错误,答案选B。

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v (H2O)为0.025 mol/(L·min),下列判断不正确的是( )
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v (H2O)为0.025 mol/(L·min),下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/mol/L | 0.1 | 0.2 | 0.2 |
C(CO2)/mol/L | 0.1 | 0.1 | 0.2 |
A. 平衡时,乙中CO2的转化率大于50%
B. 当反应平衡时,丙中c(CO2)是甲中的2倍
C. 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同