题目内容
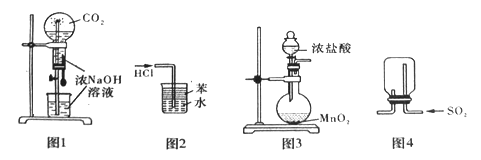
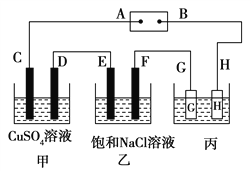
【题目】如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
(1)电极A是__________________(填“正极”或“负极”)。
(2)甲装置中电解反应的总化学方程式是_______________。
(3)若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,求所得溶液在25℃时的pH=__________________。
(4)欲用丙装置给铜镀银。G应该是___(填“银”或“铜”),电镀液的主要成分是______(填化学式)。
【答案】 正极 2CuSO4+2H2O电解2Cu+O2↑+2H2SO4 12 银 AgNO3
【解析】(1)F极附近显红色,说明该电极附近溶液显碱性,即F电极是阴极。则B是电源的负极、A是电源的正极,C是阳极、D是阴极、E是阳极;(2)惰性电极电解硫酸铜,阴极和阳极的放电离子是铜离子和OH-,所以总的反应式为2CuSO4+2H2O电解2Cu+O2↑+2H2SO4;(3)惰性电极电解氯化钠溶液的反应式为2NaCl+2H2O电解2NaOH+H2↑+Cl2↑,阳极氯离子放电,生成氯气,物质的量为![]() =0.0025mol,所以氢氧化钠的物质的量是0.0025mol×2=0.005mol,浓度是
=0.0025mol,所以氢氧化钠的物质的量是0.0025mol×2=0.005mol,浓度是![]() =0.01mol/L,因此pH等于12;(4)B是电源的负极,则H为电镀池的阴极,G为阳极,欲用丙装置给铜镀银。G应该是银,电镀液的主要成分是AgNO3。
=0.01mol/L,因此pH等于12;(4)B是电源的负极,则H为电镀池的阴极,G为阳极,欲用丙装置给铜镀银。G应该是银,电镀液的主要成分是AgNO3。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】已知硫酸、氨水的密度与所加水量的关系如下图所示:

现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
硫酸 | 4 mol·L-1 | ρ1 |
2 mol·L-1 | ρ2 | |
氨水 | 4 mol·L-1 | ρ3 |
2 mol·L-1 | ρ4 |
(1)ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
(2)表中2 mol·L-1氨水的质量分数为:________。
(3)将4 mol·L-1的氨水与2 mol·L-1的硫酸等体积混合,所得溶液呈______性(填“酸”、“碱”、“中”);溶液中离子浓度从大到小的顺序是:___________________。
(4)将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______。
A.>15% B.=15% C.<15% D.无法判断
(5)100g浓度为4 mol·L-1的硫酸溶液与_____mL水混合,可以使硫酸的物质的量浓度减小到2 mol·L-1。