题目内容
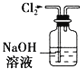
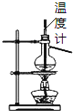
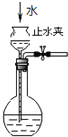
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
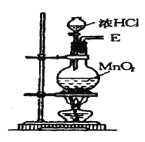
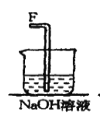
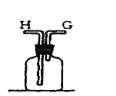
(1)该反应中生成氯气的化学方程式为:__。
(2)连接上述仪器的正确顺序是:(填各接口处的字母)E接___接___,___接___接___,___接__。___。
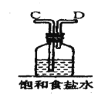
(3)在装置中,①饱和食盐水起的作用是__。
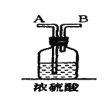
②浓硫酸起的作用是__。
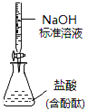
③NaOH溶液的作用是__。
(4)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:__。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O CDABHGF 吸收Cl2中HCl 干燥Cl2 吸收末反应的Cl2,防止直接排放到空气中引起污染 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
MnCl2+Cl2↑+2H2O CDABHGF 吸收Cl2中HCl 干燥Cl2 吸收末反应的Cl2,防止直接排放到空气中引起污染 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
【解析】
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,反应原理为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,需要固体-液体加热发生装置生成氯气,用饱和食盐水除去氯气中混有的氯化氢气体,通过浓硫酸除去氯气中的水蒸气,并因为氯气密度比空气大,所以用导气管长进短出的集气瓶收集氯气,最后氯气是酸性气体,并且污染空气,所以用碱液来吸收多余的氯气,防止污染空气。
MnCl2+Cl2↑+2H2O,需要固体-液体加热发生装置生成氯气,用饱和食盐水除去氯气中混有的氯化氢气体,通过浓硫酸除去氯气中的水蒸气,并因为氯气密度比空气大,所以用导气管长进短出的集气瓶收集氯气,最后氯气是酸性气体,并且污染空气,所以用碱液来吸收多余的氯气,防止污染空气。
(1)根据分析知二氧化锰跟浓盐酸反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)根据分析知仪器的正确顺序是CDABHGF,故答案为:CDABHGF;
(3)根据分析知用饱和食盐水除氯气中的氯化氢杂质气体,用浓硫酸除去氯气中的水蒸气,得到干燥的纯净的氯气,用NaOH溶液作为尾气吸收试剂,吸收氯气防止污染空气,故答案为:①吸收Cl2中HCl,②干燥Cl2,③吸收末反应的Cl2,防止直接排放到空气中引起污染;
(4)工业上用氯气和石灰乳制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案【题目】一定温度下,在三个容积均为2L的恒容密闭容器中按不同方式投入反应物,发生反应:2CO(g) + 4H2(g)CH3OCH3(g) + H2O(g) △H<0,测得反应的相关数据如下表:
容器1 | 容器2 | 容器3 | |
反应温度T/K | 600 | 600 | 500 |
反应物投入量 | 0.2mol CO 0.4mol H2 | 0.4mol CO 0.8mol H2 | 0.2mol CH3OCH3 0.2mol H2O |
平衡v(CO)/(mol·L-1·s-1) | v1 | v2 | v3 |
平衡n(H2)/(mol) | 0.2 | n2 | n3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率a | a1(CO) | a2(CO) | a3(CH3OCH3) |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是
A.v1<v2,n2>0.4B.K2=2.5×103,p2>p3
C.2p1<p3,a1(CO) >a2(CO)D.n3<0.4,a2(CO) + a3(CH3OCH3)<1