题目内容
5.(1)A元素的最高正化合价是+4价,A原子次外层上有2个电子,A原子的电子排布式是1s22s22p2.(2)B元素在气态氢化物中显-3价,气态氢化物极易溶于水,B原子的电子排布式是1s22s22p3.
(3)E原子核外占有9个轨道,且只有1个未成对电子,E离子结构示意图是
 .
.(4)F、G都是短周期元素,F2-与G3+的电子层结构相同,则F2-的电子排布式是1s22s22p6,G元素的原子序数是13.
分析 先根据原子核外电子排布规律推导出各元素:
(1)A元素的最高正价是+4价,原子次外层上有2个电子,则A为碳;
(2)B元素在气态氢化物中显-3价,气态氢化物极易溶于水,则B为氮;
(3)E原子核外占有9个轨道,且只有1个未成对电子,则E为氯;
(4)F、G都是短周期元素,F2-与G3+的电子层结构相同,则F为氧,G为铝;
然后根据题意解答.
解答 解:(1)A元素的最高正价是+4价,原子次外层上有2个电子的元素是碳,碳的基态原子的电子排布式是:1s22s22p2,故答案为:1s22s22p2;
(2)B元素在气态氢化物中显-3价,气态氢化物极易溶于水,B元素是氮,氮的基态原子的电子排布式是:1s22s22p3,故答案为:1s22s22p3;
(3)E原子核外占有9个轨道,且只有1个未成对电子,则E为氯,氯离子是氯原子得到一个电子,离子结构示意图为: ,故答案为:
,故答案为: ;
;
(4)F、G都是短周期元素,F2-与G3+的电子层结构相同,F为氧,O2-的电子排布式是1s22s22p6,G为铝,原子序数为13,故答案为:1s22s22p6;13.
点评 本题综合考查原子核外电子排布以及原子结构与元素周期表知识,侧重于基础知识的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
15.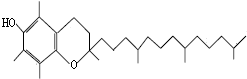 蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )
蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )
 蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )
蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )| A. | 维生素E的化学式为:C29H50O2 | |
| B. | 维生素E的还原性主要是酚羟基表现出来,若被酯化后就不具有抗氧化活性 | |
| C. | 维生素E易溶于水和乙醇、苯等有机溶剂 | |
| D. | 维生素E虽含有酚羟基,但不能与溴水反应 |
16.用金属铜制取硝酸铜,从节约原料和防止环境污染考虑,最好的方法是( )
| A. | 铜$\stackrel{浓硫酸}{→}$硝酸铜 | B. | 铜$\stackrel{稀硫酸}{→}$硝酸铜 | ||
| C. | Cu$\stackrel{Cl_{2}}{→}$CuCl2$\stackrel{AgNO_{3}}{→}$Cu(NO3)2 | D. | Cu$\stackrel{空气}{→}$CuO$\stackrel{HNO_{3}}{→}$Cu(NO3)2 |
13.将一定体积的NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液的体积为V2;则下列叙述正确的是( )
| A. | 若V1>V2,则说明HA的酸性比HB的酸性强 | |
| B. | 若V1>V2,则说明HA的酸性比HB的酸性弱 | |
| C. | 因为两种酸溶液的pH相等,故V1一定等于V2 | |
| D. | HA、HB分别和NaOH中和后,所得的溶液都一定呈中性 |
20.一定温度下,向2.0L恒容密闭容器中充入1.0mol A,经一段时间后反应A(g)?B(g)+C(g)达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(B)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 前50 s内B的平均反应速率v(B)=0.0032 mol•L-1•s-1 | |
| B. | 相同温度下,若达到平衡后向容器中继续充入A,则平衡向右移动,平衡常数增大 | |
| C. | 相同温度下,若起始时向容器中充入1.0 mol A、0.20 mol B和0.20 mol C,则达到平衡前v(正)>v(逆) | |
| D. | 若保持其他条件不变,升高温度,平衡时,平衡常数K=0.2 mol•L-1,则反应的△H<0 |
10.原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满.下表是主要化合价及原子半径数据:
请回答下列问题:
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
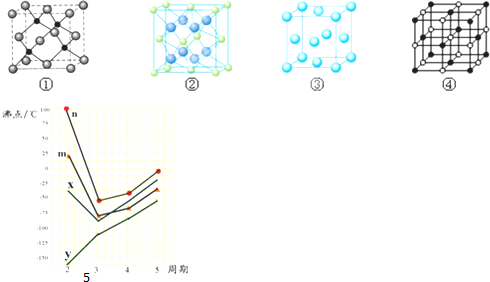
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径nm | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)

17.下列叙述正确的是( )
| A. | H2D与H2T互为同素异形体 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同、质子数相同的同种核素 | |
| D. | 短周期第 IVA与第 VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
2.相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ•mol-l.实验测得起始、平衡时的有关数据如下表:下列叙述正确的是( )
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 三个容器中反应的平衡常数均为K=2 | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$ mol/(L•min) |
