题目内容
15.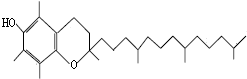 蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )
蔬菜腐烂变质或烹调时焖煮时间太长,蔬菜中的硝酸盐会被维生素E还原成亚硝酸盐,会引起亚硝酸盐中毒.如图是维生素E的结构简式.下列说法中不正确的是( )| A. | 维生素E的化学式为:C29H50O2 | |
| B. | 维生素E的还原性主要是酚羟基表现出来,若被酯化后就不具有抗氧化活性 | |
| C. | 维生素E易溶于水和乙醇、苯等有机溶剂 | |
| D. | 维生素E虽含有酚羟基,但不能与溴水反应 |
分析 维生素E中含有苯环、酚羟基和醚键,能发生加成反应、取代反应,
A.根据C原子形成4个共价键、O原子形成2个共价键、H原子形成1个共价键确定分子式;
B.酚羟基不稳定易被氧气氧化;
C.维生素E中烃基较大,导致其不易溶于无机溶剂;
D.维生素E具有酚羟基,但苯环上酚羟基邻对位没有氢原子.
解答 解:维生素E中含有苯环、酚羟基和醚键,能发生加成反应、取代反应,
A.根据C原子形成4个共价键、O原子形成2个共价键、H原子形成1个共价键确定分子式为C29H50O2,故A正确;
B.酚羟基不稳定易被氧气氧化而导致酚羟基具有还原性,若被酯化后就不具有抗氧化活性,故B正确;
C.维生素E中烃基较大,导致其不易溶于无机溶剂,根据相似相溶原理知,维生素E易溶于有机溶剂,如乙醇、苯,故C错误;
D.维生素E具有酚羟基,但苯环上酚羟基邻对位没有氢原子,所以维生素E不能和溴发生取代反应,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高考高频点,明确物质中官能团及其性质是解本题关键,注意苯酚中并不是苯环上所有氢原子都能被溴取代,为易错点.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
3.已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlCl3中的化学键类型是共价键.
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强);简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)请你预测Br与I元素的X数值的大小关系Br大于I.
(4)某化合物分子中含有S-N键,你认为该共享电子对偏向于N原子(填元素符号).
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlCl3中的化学键类型是共价键.
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强);简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)请你预测Br与I元素的X数值的大小关系Br大于I.
(4)某化合物分子中含有S-N键,你认为该共享电子对偏向于N原子(填元素符号).
20.中草药秦皮中含有的七叶树内酯结构是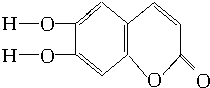 (C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
(C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
 (C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
(C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )| A. | 3 mol Br2、2 mol NaOH | B. | 3 mol Br2、4 mol NaOH | ||
| C. | 2 mol Br2、3 mol NaOH | D. | 4 mol Br2、4 mol NaOH |
7.人造象牙主要成分的结构是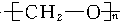 ,它是通过加聚反应制得的,则合成象牙的单体是( )
,它是通过加聚反应制得的,则合成象牙的单体是( )
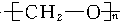 ,它是通过加聚反应制得的,则合成象牙的单体是( )
,它是通过加聚反应制得的,则合成象牙的单体是( )| A. | (CH3)2O | B. | CH3CHO | C. | HCHO | D. | C2H2和H2O |
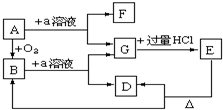 在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白:
在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白: .
.