题目内容
【题目】人体血液存在H2CO3/HCO3—、HPO42-/H2PO4—等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lg x[x表示![]() 或
或![]() ]与pH的关系如图所示。已知碳酸pKal═6.4、磷酸pKa2═7.2 (pKa═ -lgKa)。则下列说法不正确的是
]与pH的关系如图所示。已知碳酸pKal═6.4、磷酸pKa2═7.2 (pKa═ -lgKa)。则下列说法不正确的是

A. 曲线Ⅱ表示lg![]() 与pH的变化关系
与pH的变化关系
B. a~b的过程中,水的电离程度逐渐增大
C. 当c(H2CO3) ═c (HCO3—)时,c(HPO42—)=c(H2PO4—)
D. 当pH增大时,![]() 逐渐增大
逐渐增大
【答案】D
【解析】
由电离平衡H2CO3 ![]() HCO3-+H+、H2PO4-
HCO3-+H+、H2PO4- ![]() HPO42-+H+可知,随pH增大,溶液中c(OH-)增大,使电离平衡向右移动,H2CO3 /HCO3-减小,HPO42-/H2PO4-增大,所以曲线I表示lg[H2CO3 /HCO3-)]与pH的变化关系,曲线II表示lg[c(HPO42-)/c(H2PO4-)]与pH的变化关系,以此分析解答。
HPO42-+H+可知,随pH增大,溶液中c(OH-)增大,使电离平衡向右移动,H2CO3 /HCO3-减小,HPO42-/H2PO4-增大,所以曲线I表示lg[H2CO3 /HCO3-)]与pH的变化关系,曲线II表示lg[c(HPO42-)/c(H2PO4-)]与pH的变化关系,以此分析解答。
A. 根据以上分析,曲线I表示lg[H2CO3 /HCO3-)]与pH的变化关系,故A错误;
B. 曲线I表示lg[H2CO3 /HCO3-)]与pH的变化关系,a→b的过程中,c(HCO3-)逐渐增大,对水的电离促进作用增大,所以水的电离程度逐渐增大,故B错误;
C. 根据H2CO3 ![]() HCO3-+H+,Kal=
HCO3-+H+,Kal=![]() ;H2PO4-
;H2PO4- ![]() HPO42-+H+,Ka2=
HPO42-+H+,Ka2=![]() ;由题给信息可知,Ka1
;由题给信息可知,Ka1![]() Ka2,则当c(H2CO3) =c(HCO3— )时c(HPO42-)
Ka2,则当c(H2CO3) =c(HCO3— )时c(HPO42-)![]() c(H2PO4-),故C错误;
c(H2PO4-),故C错误;
D. 根据Kal=![]() ;Ka2=
;Ka2=![]() ,可得c(HCO3- )
,可得c(HCO3- )![]() c(H2PO4-)/c(HPO42-)=
c(H2PO4-)/c(HPO42-)=![]() c(H2CO3),
c(H2CO3),
当pH增大时,c(H2CO3)逐渐减小,所以c(HCO3- )![]() c(H2PO4-)/c(HPO42-)逐渐减小,故D正确。
c(H2PO4-)/c(HPO42-)逐渐减小,故D正确。
故答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】I.现用物质的量浓度为0.100 0 mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
(1)从下表中选出正确选项______________


(2)某学生的操作步骤如下:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴部分充满溶液;
D.取标准NaOH溶液注入碱式滴定管至“0”刻度以上 2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是____→___→___→___→A→___(用字母序号填写)______________。判断到达滴定终点的实验现象是_____________________________________。
(3)若滴定达终点时,滴定管中的液面如上图所示,正确的读数为__________
A.22.30 mL B.23.65 mL
C.22.35 mL D.23.70 mL
(4)由于错误操作,使得上述所测盐酸溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.酸式滴定管用蒸馏水洗净后立即取用25.00 mL待测酸溶液注入锥形瓶进行滴定
C.碱式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.用酸式滴定管量取待测盐酸时,取液前有气泡,取液后无气泡
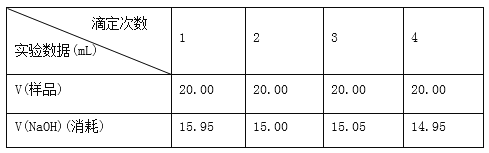
(5)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 20.00 | 1.02 | 21.03 |
2 | 20.00 | 2.00 | 21.99 |
3 | 20.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品的浓度是________________ 。
【题目】(1)汽车尾气中的CO、NOx、碳氢化合物是大气污染物。使用稀土等催化剂能将CO、NO转化成无毒物质。
已知:N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
2C(s)+O2(g)=2CO(g) △H2=-221 kJ/mol
C(s)+O2(g)=CO2(g) △H3=-393.5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式为: _______________。
(2)工业上可以在恒容密闭容器中采用下列反应制备甲醇:CO(g)+2H2(g)![]() CH3OH(g),下表所列数据为该反应在不同温度下的化学平衡常数:
CH3OH(g),下表所列数据为该反应在不同温度下的化学平衡常数:
温度/℃ | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
①反应的平衡常数表达式为K=______。由上表数据判断,该反应的△H_______ 0(填“>”、“=”或“<”)。升高温度,正反应速率________填“增大”、“减小”或“不变”)。
②某温度下,将2molCO和6molH2充入一个容积为2L的密闭容器中,达到平衡时c(H2)=1.4mol/L,则CO的转化率为_______,此时的温度为_______。
③欲提高CO的转化率,可采取的措施是______ 。(填序号)
A.升温 B.加入更高效的催化剂 C.恒容条件下充入CO
D.恒容条件下充入H2 E.恒容条件下充入氦气 F.及时移走CH3OH