题目内容
19.已知使36g焦炭发生不完全燃烧,所得气体中CO占$\frac{1}{3}$体积,CO2占$\frac{2}{3}$体积,已知:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-Q1kJ/mol,
CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-Q2kJ/mol
与这些焦炭完全燃烧相比较,损失的热量是中正确的是( )
| A. | $\frac{1}{2{Q}_{2}}$ kJ | B. | Q2kJ | C. | $\frac{1}{3({Q}_{1}+{Q}_{2})}$kJ | D. | $\frac{1}{3{Q}_{1}}$kJ |
分析 盖斯定律指若是一个反应可以分步进行,则各步反应的吸收或放出的热量总和与这个反应一次发生时吸收或放出的热量相同.
36g碳不完全燃烧与这些碳完全燃烧相比损失的热量为生成的一氧化碳燃烧放出的热量.根据碳原子守恒计算出一氧化碳的物质的量,再根据一氧化碳燃烧的热化学方程式计算,即可解答.
解答 解:36g碳的物质的量为n=$\frac{m}{M}$=$\frac{36g}{12g/mol}$=3mol,不完全燃烧所得气体中,CO占三分之一体积,根据碳原子守恒,求得CO的物质的量为3mol×$\frac{1}{3}$=1mol,根据CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-Q2kJ/mol,1molCO燃烧放出的热量为Q2kJ,
故选B.
点评 本题主要考查反应热的计算,考查了盖斯定律的原理理解运用,本题关键点是碳不完全燃烧损失的热量为生成的一氧化碳燃烧放出的热量,题目难度不大.

练习册系列答案
相关题目
12.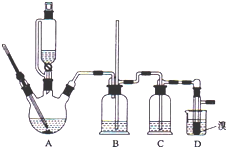 实验室制备 1,2-二溴乙烷的反应原理如下:
实验室制备 1,2-二溴乙烷的反应原理如下:
CH3CH2OH→CH2=CH2+H2OC H2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是d;(填正确选 项前的字母)
a.引发反应b.加快反应速度c.防止乙醇挥发d.减少副产物乙醚生成
(2)在装置 C 中应加入NaOH溶液,其目的是吸收反应中可能生成的酸性气体 (填正确选项前的字母) a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的 Br2,最好用b洗涤除去(填正确选项前的字母);
a.水b.氢氧化钠溶液c.碘化钠溶液d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去蒸馏;
(7)反应过程中应用冷水冷却装置 D,其主要目的是冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
 实验室制备 1,2-二溴乙烷的反应原理如下:
实验室制备 1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2+H2OC H2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是d;(填正确选 项前的字母)
a.引发反应b.加快反应速度c.防止乙醇挥发d.减少副产物乙醚生成
(2)在装置 C 中应加入NaOH溶液,其目的是吸收反应中可能生成的酸性气体 (填正确选项前的字母) a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的 Br2,最好用b洗涤除去(填正确选项前的字母);
a.水b.氢氧化钠溶液c.碘化钠溶液d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去蒸馏;
(7)反应过程中应用冷水冷却装置 D,其主要目的是冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 用排饱和食盐水法收集Cl2 | |
| B. | 冰镇的啤酒打开后泛起泡沫 | |
| C. | 加压有利于合成氨反应 | |
| D. | 金属铝、铁与同浓度的盐酸反应铝的速度快 |
4.下列应用或事实与胶体的性质没有关系的是( )
| A. | 工厂利用高压电除尘,有利于减轻雾霾和预防大气污染 | |
| B. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 | |
| C. | 过滤泥水混合物,用激光笔照射滤液,能产生光亮的通路 | |
| D. | 江河入海出容易形成三角洲,如长江三角洲和黄河三角洲的形成 |
8.分类方法在化学学科的发展中起到了非常重要的作用.下列分类标准合理的是( )
| A. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等 | |
| B. | 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| D. | 根据氧化物中是否含有金属元素将氧化物分为酸性氧化物和碱性氧化物 |
9.下列物质中,属于碱性氧化物的是( )
| A. | CaO | B. | CO | C. | P2O5 | D. | CO2 |
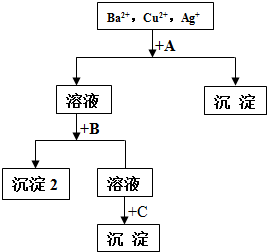 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(写出最佳答案)
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(写出最佳答案)