��Ŀ����
����Ŀ��I.��ȩ��ľ�ļӹ���ҽҩ�ȷ�������Ҫ��;���״�ֱ�������ǹ�ҵ�Ϻϳɼ�ȩ���·������Ʊ������漰����Ҫ��Ӧ���£�
��ӦI��CH3OH(g)![]() HCHO(g)+H2(g) ��H1=+85.2kJ/mol
HCHO(g)+H2(g) ��H1=+85.2kJ/mol
��ӦII��CH3OH(g)+![]() O2(g)
O2(g)![]() HCHO(g)+H2O(g) ��H2
HCHO(g)+H2O(g) ��H2
��ӦIII��2H2(g)+O2(g)![]() 2H2O(g) ��H3=-483.6kJ/mol
2H2O(g) ��H3=-483.6kJ/mol
(1)���㷴Ӧ��ķ�Ӧ����H2=_____________________________��
(2)750K�£��ں����ܱ������У�������ӦCH3OH(g)![]() HCHO(g)+H2(g��������ʼѹǿΪP0���ﵽƽ��ת����Ϊ������ƽ��ʱ����ѹǿPƽ=___________(�ú�P0������ʽ�ӱ�ʾ)����P0=101kPa�������=50.0%�����㷴Ӧƽ�ⳣ��Kp=___________kPa(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������������������Ӧ)��
HCHO(g)+H2(g��������ʼѹǿΪP0���ﵽƽ��ת����Ϊ������ƽ��ʱ����ѹǿPƽ=___________(�ú�P0������ʽ�ӱ�ʾ)����P0=101kPa�������=50.0%�����㷴Ӧƽ�ⳣ��Kp=___________kPa(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������������������Ӧ)��
II.CO2�����������壬Ҳ����Ҫ�Ļ���ԭ�ϣ���CO2Ϊԭ�Ͽɺϳɶ����л��
(3)CO2����������ϩ����֪��2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ��H��QkJ/mol��һ�������£�����ͬ��Ͷ�ϱ�X[X��
CH2=CH2(g)+4H2O(g) ��H��QkJ/mol��һ�������£�����ͬ��Ͷ�ϱ�X[X��![]() ]��ij�ݻ��ɱ�ĺ�ѹ�ܱ������г���CO2��H2����ò�ͬͶ�ϱ�ʱCO2��ת�������¶ȵĹ�ϵ��ͼ��ʾ��
]��ij�ݻ��ɱ�ĺ�ѹ�ܱ������г���CO2��H2����ò�ͬͶ�ϱ�ʱCO2��ת�������¶ȵĹ�ϵ��ͼ��ʾ��

��X1_____X2����������������������ͬ����Q_____0��
��ͼ��A��B��C�����Ӧ��ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ_____��
(4)�����£���NaOH��Һ��CO2�����������Խ���̼�ŷţ����ҿɵõ���Ҫ�Ļ�����ƷNa2CO3��
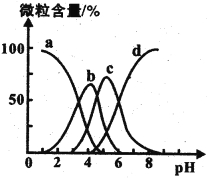
����ij�β���õ�pH��10����Һ������Һ��c(CO32-)��c(HCO3-)=_____[������K1(H2CO3)=4.4��10��7��K2(H2CO3)=5��10��11]��
������5L Na2CO3��Һ��23.3g BaSO4����ȫ��ת��ΪBaCO3�������õ�Na2CO3��Һ�����ʵ���Ũ������Ϊ__________��[��֪��������Ksp(BaSO4)=1��10��7��Ksp(BaCO3)=2.5��10��6]��(������Һ������ı仯)
���𰸡�-156.6kJ/mol P0(1+��) 50.5 > < KA>KB��KC 1��2 0.52mol/L
��������
(1)���ݸ�˹���ɣ���ӦI+![]() ��ӦIII�÷�Ӧ�ݴ˼�����H2��
��ӦIII�÷�Ӧ�ݴ˼�����H2��
(2)���ݺ���ʱ�����ѹǿ�ȵ�����������ʵ����ıȼ���ƽ��ʱ��ѹǿ������ƽ�ⳣ������ʽ������ƽ�ⳣ����
(3)�ٵ���������һ��ʱ�������H2��Խ�࣬CO2ת����Խ�ߣ���Ӧ��XԽ����X1��X2����������������ʱ�����ͼ���֪���¶����ߣ�CO2��ת���ʽ��ͣ�����֪�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���ݴ˽��з�����
�ڽ��ͼ���֪�÷�Ӧ����ӦΪ���ȷ�Ӧ�����¶����ߣ���ѧƽ�ⳣ������С�����һ�ѧƽ�ⳣ��ֻ���¶��йأ�
(4)��������pH=10���ɼ���c(H+)=1��10-10mol/L����HCO3-![]() CO32-+H+�ɵã�Ka2=
CO32-+H+�ɵã�Ka2=![]() =5��10��11������
=5��10��11������![]() =1��2��
=1��2��
����������Ҫ���ʵ���Ũ��Ϊxmol/L��Na2CO3��Һ����BaSO4��ȫ�ܽ��23.3g BaSO4�����ʵ���Ϊn(BaSO4)= 23.3g��233g/mol=0.1mol������5L��Һ��c(SO42-)=0.1mol ��5L=0.02mol/L����ʱ��Һ��c(CO32-)=(x-0.02)mol/L����BaSO4+CO32-=BaCO3+SO42-��֪���˷�Ӧ�Ļ�ѧƽ�ⳣ��K=![]() =0.04=
=0.04=![]() ���ݴ˽��м��㡣
���ݴ˽��м��㡣
(1)I+![]() ��III�������ɵ�CH3OH(g)+
��III�������ɵ�CH3OH(g)+![]() O2(g)
O2(g)![]() HCHO(g)+H2O(g) ��H2=��H1+
HCHO(g)+H2O(g) ��H2=��H1+![]() ����H3=-156.6kJ/mol��
����H3=-156.6kJ/mol��
(2)�����ں���ʱ�����ѹǿ�ȵ�����������ʵ����ıȼ���ƽ��ʱ��ѹǿ������ʼѹǿΪP0���ﵽƽ��ת����Ϊ����
CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
��ʼ(mol) 1 0 0
�仯(mol) a a a
ƽ��(mol) 1-a a a
ѹǿ֮�ȵ������ʵ���֮�ȣ���p0��Pƽ=1(1+a)��Pƽ=p0(1+a)����P0=101kPa�������=50.0%���÷�Ӧƽ�ⳣ��Kp=![]() =50.5 kPa��
=50.5 kPa��
(3)�ٵ���������һ��ʱ�������H2��Խ�࣬CO2ת����Խ�ߣ���Ӧ��XԽ����X1>X2����������������ʱ�����ͼ���֪���¶����ߣ�CO2��ת���ʽ��ͣ�����֪�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����Q��0��
�ڽ��ͼ���֪�÷�Ӧ������ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ����÷�Ӧ�Ļ�ѧƽ�ⳣ����С�����һ�ѧƽ�ⳣ��ֻ���¶��йأ�����ͼ��֪A����¶ȵ���B��C���㣬����B��C�����¶���ͬ���������Ӧ��ƽ�ⳣ���Ĵ�С��ϵΪ��KA>KB=KC��
(4)��)��������pH=10���ɼ���c(H+)=1��10-10mol/L����HCO3-![]() CO32-+H+�ɵã�Ka2=
CO32-+H+�ɵã�Ka2=![]() =5��10��11������
=5��10��11������![]() =1��2��
=1��2��
����������Ҫ���ʵ���Ũ��Ϊxmol/L��Na2CO3��Һ����BaSO4��ȫ�ܽ��23.3g BaSO4�����ʵ���Ϊn(BaSO4)= 23.3g��233g/mol=0.1mol������5L��Һ��c(SO42-)=0.1mol ��5L=0.02mol/L����ʱ��Һ��c(CO32-)=(x-0.02)mol/L����BaSO4+CO32-=BaCO3+SO42-��֪���˷�Ӧ�Ļ�ѧƽ�ⳣ��K=![]() =0.04=
=0.04=![]() ��
��
����������Ҫ���ʵ���Ũ��Ϊxmol/L��Na2CO3��Һ����BaSO4��ȫ�ܽ������5L��Һ��c��SO42-��=0.02mol/L����ʱ��Һ��c(CO32-)=(x-0.02)mol/L����BaSO4+CO32-=BaCO3+SO42-��֪���˷�Ӧ�Ļ�ѧƽ�ⳣ��K=![]() =0.04=
=0.04=![]() �����x=0.52mol/L��
�����x=0.52mol/L��