题目内容
【题目】氮、碳氧化物的排放会对环境造成污染。多年来化学工作者对氮、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g)![]() N2O2(g) (快) H1<0;
N2O2(g) (快) H1<0;
v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g)![]() 2NO2(g) (慢) H2< 0;
2NO2(g) (慢) H2< 0;
v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
①在两步的反应中,哪一步反应的活化能更大___(填“第一步”或“第二步”)。
②一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
II.(1)利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中部分反应的热化方程式为:
① CH4(g)=C(s)+2H2(g) ΔH1>0
② CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2>0
③ CO(g)+H2(g)=C(s)+H2O(g) ΔH3<0
则反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=______________________(用含 ΔH1 、ΔH2 、 ΔH3的代数式表示)若固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。


同温度下CO2的平衡转化率大于CH4的平衡转化率,原因是_________。
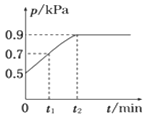
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g) + CH4(g)![]() 2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填 “大于”“小于”或“等于”)。已知气体分压(p 分)=气体总压(p 总)× 气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x 点对应温度下反应的平衡常数Kp=__________________。
2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填 “大于”“小于”或“等于”)。已知气体分压(p 分)=气体总压(p 总)× 气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x 点对应温度下反应的平衡常数Kp=__________________。
III.根据2CrO42﹣+2H+ ![]() Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的_________极,电解制备过程的总反应化学方程式为_________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为_________。若选择用熔融K2CO3作介质的甲烷(CH4)燃料电池充当电源,则负极反应式为________________。
Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的_________极,电解制备过程的总反应化学方程式为_________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为_________。若选择用熔融K2CO3作介质的甲烷(CH4)燃料电池充当电源,则负极反应式为________________。
【答案】第二步 ![]() ΔH1 +ΔH2 -ΔH3 CO2发生了其他副反应 大于
ΔH1 +ΔH2 -ΔH3 CO2发生了其他副反应 大于 ![]() 负 4Na2CrO4+4H2O
负 4Na2CrO4+4H2O![]() 2Na2Cr2O7+4NaOH+2H2↑+O2↑ (2﹣
2Na2Cr2O7+4NaOH+2H2↑+O2↑ (2﹣![]() )×100% CH4﹣8e﹣+4CO32﹣=5CO2+2H2O
)×100% CH4﹣8e﹣+4CO32﹣=5CO2+2H2O
【解析】
Ⅰ. ①总反应的快慢由反应慢的一步决定,慢反应所需要的活化能更大,故答案为:第二步;
②因为反应达到平衡状态,所以v1正=v1逆,v2正=v2逆,所以v1正v2正=v1逆v2逆,即k1正c2(NO)×k2正c(N2O2)c(O2)=k1逆c(N2O2)k2正c(N2O2),则![]() ,故答案为:
,故答案为:![]() ;
;
Ⅱ.(1)将已知的三个反应重新组合,反应1+2-3,得到反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),根据盖斯定律得ΔH=ΔH1 + ΔH2 - ΔH3,反应方程式中CH4和CO2的化学计量数之比为1:1,投料比也为1:1,因此二者转化率应该相同,但是所给的转化率图像中,CO2转化率曲线高于CH4转化率曲线,可能是CO2发生了一些副反应造成的,故答案为:ΔH1 +ΔH2-ΔH3;CO2发生了其他副反应;
2CO(g)+2H2(g),根据盖斯定律得ΔH=ΔH1 + ΔH2 - ΔH3,反应方程式中CH4和CO2的化学计量数之比为1:1,投料比也为1:1,因此二者转化率应该相同,但是所给的转化率图像中,CO2转化率曲线高于CH4转化率曲线,可能是CO2发生了一些副反应造成的,故答案为:ΔH1 +ΔH2-ΔH3;CO2发生了其他副反应;
(2) 反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)是个气体体积增大的反应,压强越大,CH4的转化率越小,由图可知相同温度下,P1条件下的转化率大于P2,则P1小于P2,压强为P2时,在Y点反应未达到平衡,则反应正向移动,所以v(正)>v(逆),由图可知该温度下X所处条件下的平衡时甲烷的转化率为50%,则有:
2CO(g)+2H2(g)是个气体体积增大的反应,压强越大,CH4的转化率越小,由图可知相同温度下,P1条件下的转化率大于P2,则P1小于P2,压强为P2时,在Y点反应未达到平衡,则反应正向移动,所以v(正)>v(逆),由图可知该温度下X所处条件下的平衡时甲烷的转化率为50%,则有:
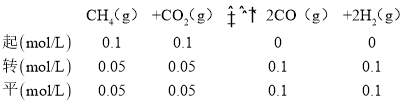
总物质的量=0.3mol,总压为P2,其平衡常数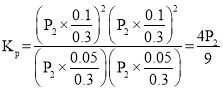 ,故答案为:大于;
,故答案为:大于;![]() ;
;
Ⅲ. 根据2CrO42-+2H+===Cr2O72-+H2O,电解Na2CrO4溶液制取Na2Cr2O7,应在酸性条件下进行,即右侧电极生成H+,则消耗OH-,发生氧化反应,右侧为阳极,则左侧为阴极,电解电源的负极,电解制备过程的总反应方程式为4Na2CrO4+4H2O![]() 2Na2Cr2O7+4NaOH+2H2↑+O2↑,设加入反应容器内的Na2CrO4为1mol,反应过程中有x mol Na2CrO4转化为Na2Cr2O7,则阳极区剩余Na2CrO4为(1-x)mol,对应的n(Na)=2(1-x)mol,n(Cr)=(1-x)mol,生成的Na2Cr2O7为
2Na2Cr2O7+4NaOH+2H2↑+O2↑,设加入反应容器内的Na2CrO4为1mol,反应过程中有x mol Na2CrO4转化为Na2Cr2O7,则阳极区剩余Na2CrO4为(1-x)mol,对应的n(Na)=2(1-x)mol,n(Cr)=(1-x)mol,生成的Na2Cr2O7为![]() mol,对应的n(Na)=x mol,n(Cr)=x mol,根据Na与Cr的物质的量之比为a:b,解得x=
mol,对应的n(Na)=x mol,n(Cr)=x mol,根据Na与Cr的物质的量之比为a:b,解得x=![]() ,转化率为
,转化率为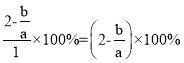 。
。
若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为CH4﹣8e﹣+4CO32﹣=5CO2+2H2O,故答案为;负;4Na2CrO4+4H2O![]() 2Na2Cr2O7+4NaOH+2H2↑+O2↑;(2﹣
2Na2Cr2O7+4NaOH+2H2↑+O2↑;(2﹣![]() )×100%;CH4﹣8e﹣+4CO32﹣=5CO2+2H2O。
)×100%;CH4﹣8e﹣+4CO32﹣=5CO2+2H2O。