题目内容
【题目】“绿水青山就是金山银山”,研究NO2、NO、CO、NO2- 等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2 + CO ![]() CO2 + NO 该反应的平衡常数为K1(下同)
CO2 + NO 该反应的平衡常数为K1(下同)
每1mol下列物质分解为气态基态原子消耗能量分别为
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+179.5 kJ/mol K2
2NO(g) ΔH=+179.5 kJ/mol K2
③2NO(g) +O2(g)![]() 2NO2(g) ΔH=-112.3 kJ/mol K3
2NO2(g) ΔH=-112.3 kJ/mol K3
试写出NO与CO反应生成无污染物气体的热化学方程式____________________________以及此热化学方程式的平衡常数K=____________(用K1、K2、K3表示)
(2)污染性气体NO2与CO在一定条件下的反应为:2NO2+4CO![]() 4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的![]() ,则反应开始到平衡时CO的平均反应速率v(CO)=________。
,则反应开始到平衡时CO的平均反应速率v(CO)=________。
若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围________________。
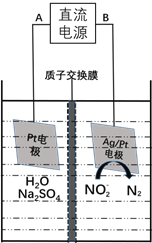
(3)电化学降解NO2-的原理如下图:
①电源的负极是____________(填A或B)阴极反应式为________________。
②若电解过程中转移了6mol电子,则膜两侧电解液的质量变化差![]() 为_____g。
为_____g。
【答案】 ![]()
![]()
![]() 0.008mol/(L·s) 0≤a<0.8(或a<0.8) B
0.008mol/(L·s) 0≤a<0.8(或a<0.8) B ![]() (或
(或![]() ) 32
) 32
【解析】(1)根据焓变=反应物总键能-生成物总键能,则反应①NO2 (g)+ CO(g)![]() CO2 (g)+ NO(g) ΔH1=(812+1076-1490-632)kJ/mol =-234 kJ/mol,②N2(g)+O2(g)
CO2 (g)+ NO(g) ΔH1=(812+1076-1490-632)kJ/mol =-234 kJ/mol,②N2(g)+O2(g) ![]() 2NO(g) ΔH2=+179.5 kJ/mol ;③2NO(g) +O2(g)
2NO(g) ΔH2=+179.5 kJ/mol ;③2NO(g) +O2(g)![]() 2NO2(g) ΔH3=-112.3 kJ/mol ;根据盖斯定律,由③+①×2-②得反应2NO(g) + 2CO(g)= N2(g)+ 2CO2 (g) ΔH=ΔH3+ΔH1×2-ΔH2 =-112.3 kJ/mol +(-234 kJ/mol)×2-179.5 kJ/mol =-759.8 kJ/mol;当总反应式相加时平衡常数相乘、相减时相除、成倍时为幂,则平衡常数K=
2NO2(g) ΔH3=-112.3 kJ/mol ;根据盖斯定律,由③+①×2-②得反应2NO(g) + 2CO(g)= N2(g)+ 2CO2 (g) ΔH=ΔH3+ΔH1×2-ΔH2 =-112.3 kJ/mol +(-234 kJ/mol)×2-179.5 kJ/mol =-759.8 kJ/mol;当总反应式相加时平衡常数相乘、相减时相除、成倍时为幂,则平衡常数K=![]() ;
;
(2)设达到平衡时CO的浓度改变x,则:
2NO2 + 4CO![]() 4CO2 + N2
4CO2 + N2
起始浓度(mol/L):0.1 0.2 0 0
改变浓度(mol/L): x 2x 2x ![]() x
x
平衡浓度(mol/L):0.1-x 0.2-2x 2x ![]() x
x
故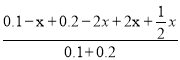 =
=![]() ,解得x=0.02mo/L,v(CO)=
,解得x=0.02mo/L,v(CO)= ![]() =0.008mol/(L·s);
=0.008mol/(L·s);
K=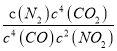 =
=![]() ;若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,则Q=
;若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,则Q=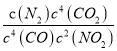 =
=![]() <K=
<K=![]() ,解得a<0.8,a的取值范围为0≤a<0.8或a<0.8;(3)根据电化学降解NO2-的原理图可知,Ag/Pt电极上NO2-转化为N2,氮元素化合价从+3价降为0价,被还原,发生还原反应,作为阴极,则电源B为负极,故①电源的负极是B,阴极反应式为:2NO2-+6e-+4H2O=N2↑+8OH-或2NO2-+6e-+8H+=N2↑+4H2O;②根据图示装置,阳极反应为2H2O-4e-=O2↑+4H+,转移6mol电子时,阳极消耗3mol水,产生6molH+进入阴极室,阳极室质量减少54g;阴极反应为2NO2-+6e-+8H+=N2↑+4H2O,阴极室中放出1molN2(28g),同时有6molH+(6g)进入阴极室,因此阴极室质量减少22g,膜两侧电解液的质量变化差(△m左-△m右)=54g-22g=32g。
,解得a<0.8,a的取值范围为0≤a<0.8或a<0.8;(3)根据电化学降解NO2-的原理图可知,Ag/Pt电极上NO2-转化为N2,氮元素化合价从+3价降为0价,被还原,发生还原反应,作为阴极,则电源B为负极,故①电源的负极是B,阴极反应式为:2NO2-+6e-+4H2O=N2↑+8OH-或2NO2-+6e-+8H+=N2↑+4H2O;②根据图示装置,阳极反应为2H2O-4e-=O2↑+4H+,转移6mol电子时,阳极消耗3mol水,产生6molH+进入阴极室,阳极室质量减少54g;阴极反应为2NO2-+6e-+8H+=N2↑+4H2O,阴极室中放出1molN2(28g),同时有6molH+(6g)进入阴极室,因此阴极室质量减少22g,膜两侧电解液的质量变化差(△m左-△m右)=54g-22g=32g。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案


