题目内容
【题目】甲烷作为一种新能源应用广泛,请回答下列问题:
(1)竖炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g) =2CO(g)+2H2(g) △H=260kJ·mol-1
2CO(g)+O2(g) = 2CO2(g) △H= -566kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为____________________
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液)通过装置Ⅱ实现铁棒上镀铜

①a处应通入_________(填CH4或O2),b处电极上发生的电极反应式是______;
②电镀结束后,装置Ⅰ中溶液的pH______。(填写变大、变小或不变,下同),装置Ⅱ中Cu2+的物质的量是________。
【答案】 2CH4(g)+O2(g)=2CO(g)+4H2(g) △H=-46 kJ·mol-1 CH4 O2+2H2O+4e-=4OH- 变小 不变
【解析】试题分析:本题考查盖斯定律的应用,燃料电池和电镀,多池串联装置的分析。
(1)将反应编号:CH4(g)+CO2(g) =2CO(g)+2H2(g)△H=260kJ·mol-1(①式)
2CO(g)+O2(g) = 2CO2(g) △H= -566kJ·mol-1(②式)
应用盖斯定律,将①式![]() 2+②式得,2CH4(g)+O2(g)=2CO(g)+4H2(g)ΔH=(260kJ/mol)
2+②式得,2CH4(g)+O2(g)=2CO(g)+4H2(g)ΔH=(260kJ/mol)![]() 2+(-566kJ/mol)=-46kJ/mol,CH4与O2反应生成CO和H2的热化学方程式为:2CH4(g)+O2(g)=2CO(g)+4H2(g)ΔH=-46kJ/mol。
2+(-566kJ/mol)=-46kJ/mol,CH4与O2反应生成CO和H2的热化学方程式为:2CH4(g)+O2(g)=2CO(g)+4H2(g)ΔH=-46kJ/mol。
(2)装置II实现铁棒上镀铜,Fe电极为阴极,Cu电极为阳极,Fe电极与a处的电极相连,a处电极为燃料电池的负极,b处电极为燃料电池的正极。
①a处电极为燃料电池的负极,a处应通入CH4。b处应通入O2,电解质溶液为KOH溶液,则b处电极上的电极反应式是:O2+4e-+2H2O=4OH-。
②装置I中甲烷燃料电池的电池反应为:CH4+2O2+2KOH=K2CO3+3H2O,KOH被消耗,电镀结束装置I中溶液的pH变小。装置II中Fe电极上的电极反应式为Cu2++2e-=Cu,Cu电极上的电极反应式为Cu-2e-=Cu2+,装置II电镀时Cu2+的物质的量不变。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】“绿水青山就是金山银山”,研究NO2、NO、CO、NO2- 等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2 + CO ![]() CO2 + NO 该反应的平衡常数为K1(下同)
CO2 + NO 该反应的平衡常数为K1(下同)
每1mol下列物质分解为气态基态原子消耗能量分别为
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+179.5 kJ/mol K2
2NO(g) ΔH=+179.5 kJ/mol K2
③2NO(g) +O2(g)![]() 2NO2(g) ΔH=-112.3 kJ/mol K3
2NO2(g) ΔH=-112.3 kJ/mol K3
试写出NO与CO反应生成无污染物气体的热化学方程式____________________________以及此热化学方程式的平衡常数K=____________(用K1、K2、K3表示)
(2)污染性气体NO2与CO在一定条件下的反应为:2NO2+4CO![]() 4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的![]() ,则反应开始到平衡时CO的平均反应速率v(CO)=________。
,则反应开始到平衡时CO的平均反应速率v(CO)=________。
若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围________________。
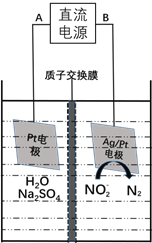
(3)电化学降解NO2-的原理如下图:
①电源的负极是____________(填A或B)阴极反应式为________________。
②若电解过程中转移了6mol电子,则膜两侧电解液的质量变化差![]() 为_____g。
为_____g。
【题目】已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
下列推断正确的是
A. 25℃时,同浓度的下列溶液 pH 关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
B. 若25℃时某溶液中c(CO32-)=c(HCO3-),则此溶液中 c(H+)=4.7×10-11 mol·L-1
C. 若某溶液中c(CO32-)=c(HCO3-),往该溶液中滴入盐酸, HCO3-比CO32-更易结合H+
D. 25℃时pH=9的CH3COONa和NaOH溶液,水电离出的c(H+)均为1×10-9mol·L-1

