题目内容
8.下列叙述中,正确的是( )| A. | 植物油和裂化汽油都能使溴水褪色 | B. | 食用植物油是人体的营养物质 | ||
| C. | 汽油、煤油、卤代烃均为烃 | D. | 甲醛可大量用作食品防腐剂 |
分析 A.植物油和裂化汽油均含不饱和键;
B、糖类、油脂、蛋白质和水、无机盐是人体必须的营养物质;
C、烃是只含C、H两种元素的化合物;
D、甲醛有毒.
解答 解:A.植物油和裂化汽油均含不饱和键,则均能与溴水发生加成反应使其褪色,故A正确;
B、糖类、油脂、蛋白质和水、无机盐是人体必须的营养物质,即食用油是人体的基本营养物质之一,故B正确;
C、烃是只含C、H两种元素的化合物,汽油和煤油是多种烷烃、环烷烃的混合物,不是化合物,故不是烃;卤代烃中除了一定含有C,可能含H,还一定含Cl原子,故不是烃,故C错误;
D、甲醛有毒,能用来浸泡标本,但不能由于食品的防腐,故D错误.
故选AB.
点评 本题考查了裂化汽油、烃的辨析和甲醛的用途,应注意的是卤代烃不是烃.

练习册系列答案
相关题目
10.一定能在下列溶液中大量共存的离子组是( )
| A. | 水电离产生的c(OH-)=1×10-12 mol/L的溶液中:NH4+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32- | |
| C. | 含有大量Fe3+的溶液:SCN-、I-、K+、Br- | |
| D. | PH=1的水溶液中:Al3+、NH4+、AlO2-、Br-. |
13.将 转变为
转变为 的方法为( )
的方法为( )
 转变为
转变为 的方法为( )
的方法为( )| A. | 与足量NaOH溶液共热后,再通入CO2 | |
| B. | 与稀H2SO4共热后,加入足量Na2CO3 | |
| C. | 与稀H2SO4共热后,加入足量NaOH | |
| D. | 与足量NaOH溶液共热后,再加入稀硫酸 |
20.四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的三倍.请用化学用语回答:
(1)丙在元素周期表中的位置第三周期第VIA族
(2)乙的两种常见单质分别是O2、O3
(3)甲乙丙丁的气态氢化物水溶液显酸性的是(写化学式)H2S,HCl
(4)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是(写化学式)H2O2.此化合物可将碱性工业废水中CN-氧化为可溶性碳酸盐和氨,相应的离子方程式H2O2+CN-+OH-=CO32-+NH3
(5)实验室制备丁单质的离子方程式4H+(浓)+2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑
(6)若甲的元素符号为X.
已知:①X2(g)+2O2(g)═X2O4(l)△H=-19.5KJ/mol
②X2H4(l)+O2(g)═X2(g)+2H2O(g)△H=-534.2KJ/mol
则液态X2H4和液态的X2O4反应生成气态X2和气态H2O的热化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol.
| 甲 | 乙 | |
| 丙 | 丁 |
(2)乙的两种常见单质分别是O2、O3
(3)甲乙丙丁的气态氢化物水溶液显酸性的是(写化学式)H2S,HCl
(4)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是(写化学式)H2O2.此化合物可将碱性工业废水中CN-氧化为可溶性碳酸盐和氨,相应的离子方程式H2O2+CN-+OH-=CO32-+NH3
(5)实验室制备丁单质的离子方程式4H+(浓)+2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑
(6)若甲的元素符号为X.
已知:①X2(g)+2O2(g)═X2O4(l)△H=-19.5KJ/mol
②X2H4(l)+O2(g)═X2(g)+2H2O(g)△H=-534.2KJ/mol
则液态X2H4和液态的X2O4反应生成气态X2和气态H2O的热化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol.
18.今年3月11日,在日本大地震灾难中,福岛核电站泄漏的放射性物质中含有${\;}_{53}^{131}$I,下列有关说法正确的是( )
| A. | ${\;}_{53}^{131}$I元素中含中子数为53 | |
| B. | 它是碘元素的一种同位素 | |
| C. | ${\;}_{53}^{131}$I2的摩尔质量为262 g | |
| D. | 由此可确定碘元素相对原子质量为131 |
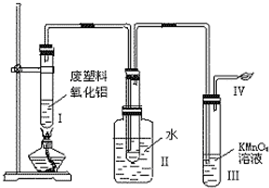 探究式学习是学生获取知识的一种重要方法,对学生的自主创新能力的培养有很大帮助.某研究性学习小组在探究塑料降解制备乙烯和汽油时做了如下实验.装置如图:
探究式学习是学生获取知识的一种重要方法,对学生的自主创新能力的培养有很大帮助.某研究性学习小组在探究塑料降解制备乙烯和汽油时做了如下实验.装置如图:
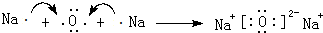 .C、D还可形成化合物D2C2,D2C2含有的化学键是离子键、非极性共价键(或离子键、共价键).
.C、D还可形成化合物D2C2,D2C2含有的化学键是离子键、非极性共价键(或离子键、共价键).