题目内容
【题目】下列各组物质中,所含分子数一定相同的是( )
A. 1 g H2和8 g O2
B. 0.1 mol HCl和2.24 L He
C. 150 ℃,1.01×105 Pa时,18 L H2O和18 L CO2
D. 常温常压下,28 g CO和6.02×1022个CO分子
【答案】C
【解析】
A.根据n=![]() 计算判断;B.He所处状态的气体摩尔体积不一定为22.4L/mol;C.相同条件下,等条件的气体含有相同分子数目;D.根据n=
计算判断;B.He所处状态的气体摩尔体积不一定为22.4L/mol;C.相同条件下,等条件的气体含有相同分子数目;D.根据n=![]() =
=![]() 计算判断。
计算判断。
A.1g氢气为![]() =0.5mol,8g氧气为
=0.5mol,8g氧气为![]() =0.25mol,二者物质的量不相等,含有分子数目不相等,选项A不符合;B.气体体积一定时,温度、压强会影响其物质的量,2.24L氦气的物质的量不一定为0.1mol,选项B不符合;C.150℃、1.01×105 Pa时,H2O和 CO2均为气体,二者物质的量相等,含有分子数目相等,选项C符合; D.28 g CO物质的量为1mol,6.02×1022个CO物质的量为0.1mol,二者含有分子数目不相等,选项D不符合,答案选C。
=0.25mol,二者物质的量不相等,含有分子数目不相等,选项A不符合;B.气体体积一定时,温度、压强会影响其物质的量,2.24L氦气的物质的量不一定为0.1mol,选项B不符合;C.150℃、1.01×105 Pa时,H2O和 CO2均为气体,二者物质的量相等,含有分子数目相等,选项C符合; D.28 g CO物质的量为1mol,6.02×1022个CO物质的量为0.1mol,二者含有分子数目不相等,选项D不符合,答案选C。

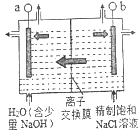
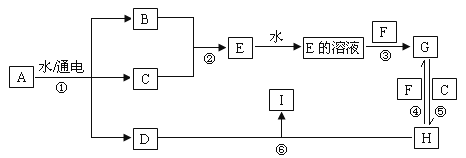
【题目】下面是实验室制备氯气并进行一系列相关实验的装置(部分夹持仪器已略)

(1)装置 B 中饱和食盐水的作用是____。
(2)装置 D 的作用是验证氯气是否具有漂白性,为此 D 中Ⅰ、Ⅱ、Ш 处依次放入物质的组合应是____(填字母编号)。
编号 | Ⅰ | Ⅱ | Ш |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水氯化钙 | 湿润的有色布条 |
c | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)设计装置 F 的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开E中活塞,将装置E 中少量溶液加入装置F中,振荡,观察到的现象是 ____,该现象____(填“能”或“不能”)说明溴单质的氧化性强于碘单质,原因是____。
(4)实验室也可以用高锰酸钾和浓盐酸反应来制备氯气,反应的化学方程式为:2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
①在化学方程式上用双线桥法标出该反应中电子转移的方向和数目 ____。
②在该反应中,氧化剂是____。
③上述反应中,有126. 4 g 的 KMnO4 参加反应,若将生成的氯气全部通入足量的石灰乳中,理论上可得到次氯酸钙多少克?_____________