题目内容
【题目】工业上,以钛铁矿(主要含FeTiO3,还含有Fe2O3 和Al2O3、SiO2等杂质)为原料制备二氧化钛并得到副产品绿矾(FeSO4·7H2O)的工艺流程如下图所示。

已知:TiO2+在一定条件下会发生水解。
回答下列问题:
(1)要提高酸浸时钛矿石的溶解速率,可行的措施是(写一条即可)_______________。黑钛液中生成的主要阳离子有TiO2+和Fe2+,步骤①主要反应的化学方程式是_________。
(2)步骤②中,加入铁粉的主要作用是_____,同时也会将部分TiO2+还原为Ti3+。
(3)向滤液2中通入空气的目的是______(用离子方程式表示)。
(4)请结合化学用语用化学平衡理论解释步骤④中加入热水稀释将TiO2+转化为Ti(OH)4 的原因:_________________。
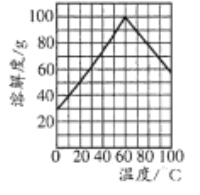
(5)副产品绿矾中含有杂质[Al2(SO4)3]。要将副产品进一步提纯,请结合右图的绿矾溶解度曲线完成提纯过程:将副产品溶于稀硫酸中,充分搅拌后,用NaOH溶液调节反应液的pH约为5,过滤沉淀后得到FeSO4溶液,______,过滤,用冰水洗涤,低温干燥,得到FeSO4·7H20晶体。
(6)用氧化还原滴定法测定制备得到的产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵[NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是_______________。
②滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol/L NH4Fe(SO4)2标准溶液24.00mL,则TiO2的质量分数为_______________。
【答案】粉碎矿石或加热反应物或及时搅拌等 FeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O 将Fe3+转化为Fe2+并防止Fe2+被氧化 4Ti3++ O2 + 2H2O
FeSO4+TiOSO4+2H2O 将Fe3+转化为Fe2+并防止Fe2+被氧化 4Ti3++ O2 + 2H2O![]() 4TiO2+ + 4H+ TiO2+在溶液中水解:TiO2+ + 3H2O
4TiO2+ + 4H+ TiO2+在溶液中水解:TiO2+ + 3H2O ![]() Ti(OH)4 + 2H+ △H>0,当加入热水稀释、升温后,平衡正向移动,生成Ti(OH)4 加热浓缩得到60℃的饱和溶液,再冷却至室温(或0℃)结晶 滴入最后滴标准溶液时, 锥形瓶内溶液变成红色, 且半分钟不褪色 96%
Ti(OH)4 + 2H+ △H>0,当加入热水稀释、升温后,平衡正向移动,生成Ti(OH)4 加热浓缩得到60℃的饱和溶液,再冷却至室温(或0℃)结晶 滴入最后滴标准溶液时, 锥形瓶内溶液变成红色, 且半分钟不褪色 96%
【解析】
(1)要提高酸浸时钛矿石的溶解速率,可增大接触面积、加热或加快搅拌;黑钛液中生成的主要阳离子有TiO2+和Fe2+,他们的存在形式是TiOSO4和FeSO4,反应的化学方程式是:FeTiO3+2H2SO4![]() FeSO4+TiOSO4+2H2O;
FeSO4+TiOSO4+2H2O;
(2)由(1)可知黑钛液中生成的主要阳离子有TiO2+和Fe2+,加入铁粉的目的除了可将部分TiO2+还原为Ti3+之外,还可将Fe3+转化为Fe2+并防止Fe2+被氧化;
(3)向滤液2中通入空气,可将三价的钛离子氧化成TiO2+,用离子方程式表示为:4Ti3++ O2 + 2H2O=4TiO2+ + 4H+
(4)TiO2+在一定条件下会发生水解生成Ti(OH)4和氢离子,溶液中存在平衡:TiO2++3H2O![]() Ti(OH)4+2H+,△H>0,当加入热水稀释、升温后,平衡正向移动,生成Ti(OH)4;
Ti(OH)4+2H+,△H>0,当加入热水稀释、升温后,平衡正向移动,生成Ti(OH)4;
(5)根据金属离子沉淀的pH值,通过滴加NaOH溶液调节pH至5.0把Al3+除去,过滤,即得到FeSO4溶液,加热浓缩得到60℃饱和溶液,然后放在冰水中冷却至室温,冷却结晶,后过滤,洗涤,低温干燥,得到FeSO4·7H20晶体;
(6)①TiO2中Ti的化合价由+4价→+3价,化合价降低,把Fe2+氧化成Fe3+,Fe3+与KSCN溶液,溶液变红,即滴定到终点的现象是:滴入最后一滴标准溶液时, 锥形瓶内溶液变成红色, 且半分钟不褪色;③依据得失电子数目守恒,有:n(Fe2+)×1=n(TiO2)×1,即n(TiO2)=n(Fe2+)=24×10-3×0.1mol=2.4×10-3mol,其质量分数为2.4×10-3×80/0.2×100%=96%;

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案