题目内容
10.下列说法不正确的是( )| A. | 豆科植物通过根瘤菌吸收空气中的氮是化学变化 | |
| B. | 化石燃料燃烧通常不释放出氮氧化合物 | |
| C. | 汽车尾气中排放的氮氧化合物是由游离态氮转化来的 | |
| D. | 植物秸秆燃烧时放出氮氧化合物,参与了氮的循环 |
分析 A.化学变化一定有新物质生成的变化;
B.化石燃料中含有氮元素,燃烧产生氮的氧化物;
C.汽油燃烧时,空气中的氮气与氧气反应生成氮的氧化物;
D.植物秸秆含有氮元素,燃烧时反应生成氮的氧化物;
解答 解:A.豆科植物通过根瘤菌吸收空气中的氮,该过程氮元素由游离态转化为化合态,有新物质生成,是化学变化,故A正确;
B.化石燃料中含有氮元素,燃烧产生氮的氧化物,所以化石燃料燃烧能够释放出氮氧化合物,故B错误;
C.汽油燃烧时,空气中的氮气与氧气反应生成氮的氧化物,故C正确;
D.植物秸秆含有氮元素,燃烧时反应生成氮的氧化物,参与了氮的循环,故D正确;
故选B.
点评 本题考查了氮的循环,熟悉含氮物质和氮的固定的概念是解题关键,注意相关知识的积累,题目难度不大.

练习册系列答案
相关题目
13.下列离子组一定能大量共存的是( )
| A. | pH=1的无色溶液中:K+、NH4+、SO42-、MnO4- | |
| B. | 水电离出的c(OH-)=10-12 mo1•L-1的溶液中:Fe2+、Ba2+、NO3-、ClO- | |
| C. | 含大量A13+的溶液中:Na+、SO42-、NO3-、[Al(OH)4]- | |
| D. | CO2的饱和溶液中:K+、Ca2+、Cl-、NO3- |
14.化学与生产、生活、社会密切相关,下列有关说法不正确的是( )
| A. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| B. | 近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| C. | 食品保鲜膜、一次性食品袋的主要成分是聚乙烯 | |
| D. | 使用纤维素和淀粉为原料制成的微生物降解塑料,可治理“白色污染” |
11.亚硝酸钠(NaNO2)是一种工业盐,实验室可用如下装置(略去部分夹持仪器)制备.

已知:①2NO+Na2O2=2NaNO2;
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排除装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶(填操作名称)、过滤可获得CuSO4•5H2O.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸溶液中有气泡产生且在试管口上方出现红棕色气体,则产物是NaNO2(注明试剂、现象).
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
①第一组实验数据出现异常,造成这种异常的原因可能是ac(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)
25°C.

已知:①2NO+Na2O2=2NaNO2;
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排除装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶(填操作名称)、过滤可获得CuSO4•5H2O.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸溶液中有气泡产生且在试管口上方出现红棕色气体,则产物是NaNO2(注明试剂、现象).
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)
25°C.
5.对于固定体积的密闭容器中进行的气体反应A(g)+B(g)?C(s)+2D(g),可以说明在恒温下已达到平衡状态的是( )
①反应容器中压强不随时间变化而变化
②A气体和B气体的生成速率相等
③混合气体的平均摩尔质量不随时间变化而变化
④反应混合气体的密度不随时间变化而变化.
①反应容器中压强不随时间变化而变化
②A气体和B气体的生成速率相等
③混合气体的平均摩尔质量不随时间变化而变化
④反应混合气体的密度不随时间变化而变化.
| A. | ③④ | B. | ②③ | C. | ①③ | D. | ①④ |
15.下列有关铝及铝合金说法错误的是( )
| A. | 氧化铝是一种高硬度、高熔沸点的化合物 | |
| B. | 铝是活泼的金属,其合金抗腐蚀能力差 | |
| C. | 铝合金具有密度小、高强度及较好的可塑性 | |
| D. | 铝合金可用于制飞机骨架等 |
2.下列关于物质性质的比较,正确的是( )
| A. | NaF、NaCl、NaBr、NaI的熔点依次升高 | |
| B. | 熔点:铯>钾>钠>钠和钾的合金 | |
| C. | 熔沸点:HI>HBr>HCl>HF | |
| D. | 热稳定性:HF>HCl>HBr>HI |
19.如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )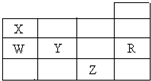

| A. | 常压下五种元素的单质中,Z单质的沸点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | W的氢化物的稳定性比X的氢化物的稳定性高 | |
| D. | Y元素的非金属性比W元素的非金属性强 |
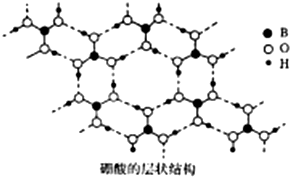 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题: [B(OH)4]-+H+.
[B(OH)4]-+H+.